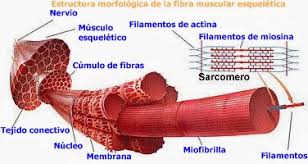
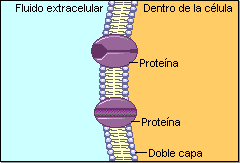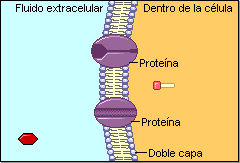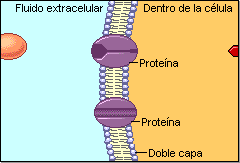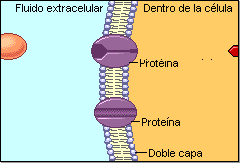
Excitación del musculo esquelético: transmisión neuromuscular y acoplamiento excitación–contracción
Transmisión de impulsos desde las terminaciones nerviosas a las fibras del musculo esquelético
La unión neuromuscular
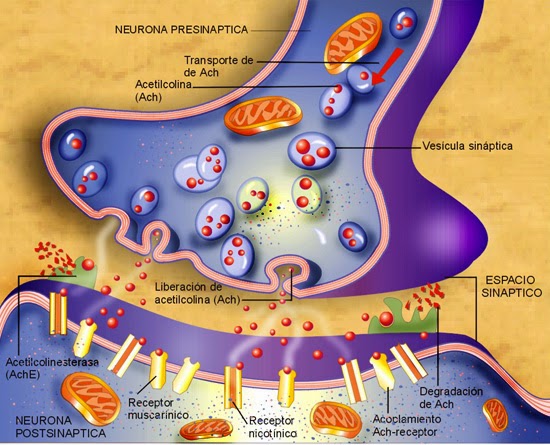
Las fibras del musculo esquelético están inervadas por fibras nerviosas mielinizadas grandes que se originan en las motoneuronas de la medula espinal. Cada fibra nerviosa estimula normalmente entre tres y varios cientos de fibras musculares esqueléticas. Cada terminación nerviosa forma una unión denominada unión neuromuscular, y el potencial de acción de la fibra muscular viaja en ambas direcciones hacia los extremos de la fibra muscular.
Secreción de acetilcolina por las terminaciones nerviosas
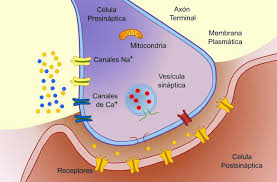
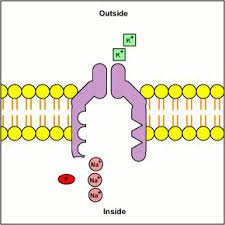
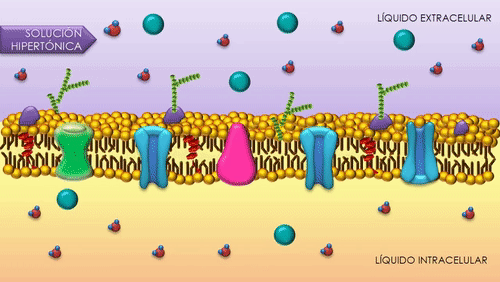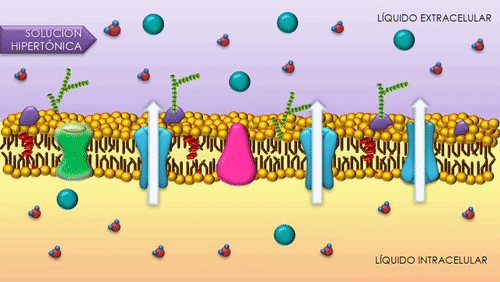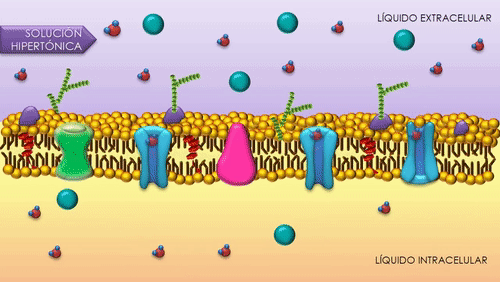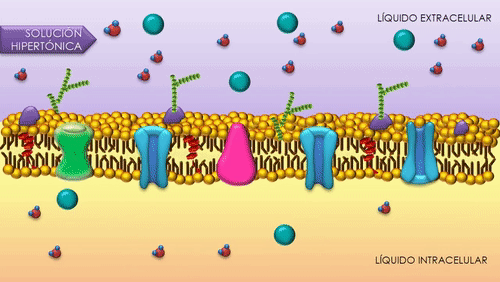
Cuando un impulso nervioso llega a la unión neuromuscular se liberan vesículas de acetilcolina hacia el espacio sináptico. En la superficie interna de la membrana neuronal hay barras densas lineales. A ambos lados de cada una de estas barras densas hay canales de calcio activados por el voltaje. Cuando el potencial de acción se propaga por la terminación, dichos canales se abren permitiendo que iones calcio difundan hacia el interior de la terminación nerviosa. Se piensa que los iones calcio ejercen una influencia de atracción sobre las vesículas de acetilcolina, desplazándolas hacia la membrana neural adyacente a las barras densas. Algunas vesículas se fusionan con la membrana neural y vacían su acetilcolina hacia el espacio sináptico mediante el proceso de exocitosis.
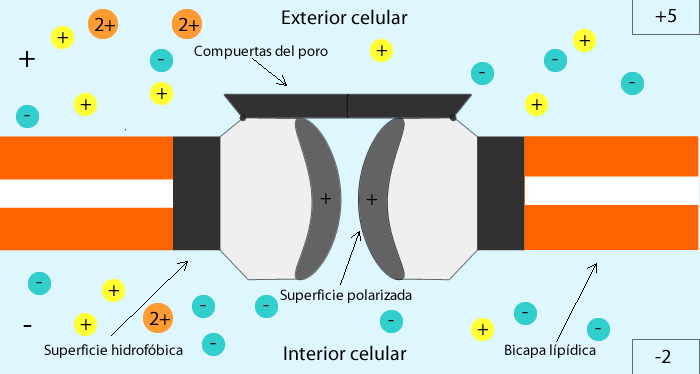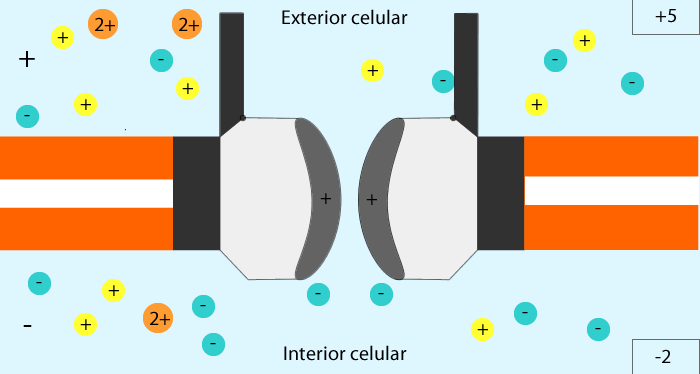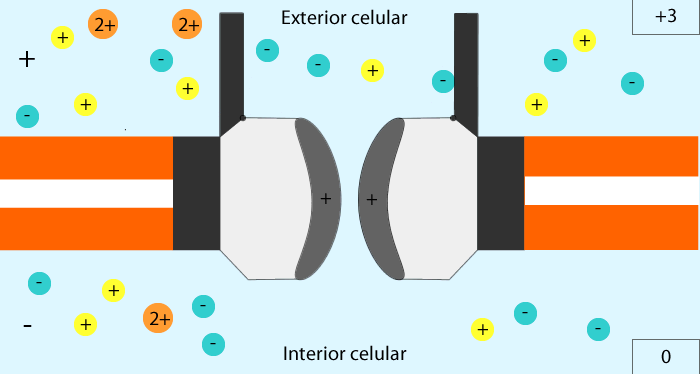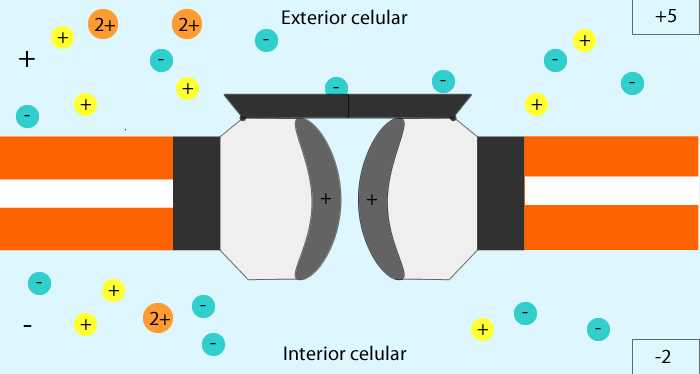
La acetilcolina abre los canales iónicos activados por acetilcolina en la membrana postsinaptica. Los canales iónicos activados por acetilcolina están localizados en la membrana muscular, inmediatamente adyacentes a las barras densas. Cuando dos moléculas de acetilcolina se unen a los receptores del canal, un cambio estructural abre el canal. El efecto principal de la apertura de los canales activados por acetilcolina es permitir que grandes cantidades de iones de sodio entran al interior de la fibra, desplazando con ellos grandes números de cragas positivas. Esto genera un cambio de potencial local en la membrana de la fibra muscular, denominada potencial de la placa terminal o potencial generador. A su vez, este potencial de la placa terminal lleva normalmente a la abertura de los canales de sodio activados por el voltaje, lo que inicia un potencial de acción en la membrana muscular y, así produce la contracción muscular.
La acetilcolina liberada en el espacio sináptico es destruida por la acetilcolinesterasa o desaparece por difusión. Una vez que se ha liberado hacia el espacio sináptico, la acetilcolina sigue activando los receptores de acetilcolina mientras persiste en el espacio. La mayor parte de la acetilcolina es destruida por la enzima acetilcolinesterasa. Una pequeña cantidad de acetilcolina difunde hacia el exterior del espacio sináptico. El breve espacio de tiempo durante el que la acetilcolina permanece en el espacio sináptico es siempre suficiente para excitar la fibra muscular en condiciones normales.
La acetilcolina produce un potencial de la placa terminal que excita la fibra muscular esquelética. La entrada de iones sodio en la fibra muscular hace que el potencial eléctrico en el interior de la fibra en la zona local de la placa terminal aumente en dirección positiva de 50 a 75 mV, generando un potencial local denominado potencial de la placa terminal. El potencial creado en la placa terminal por la estimulación con acetilcolina es, normalmente, mucho mayor que el necesario para iniciar un potencial de acción en la fibra muscular. Así, cada potencial de acción en una neurona motora conduce a la contracción de las fibras musculares.
Fármacos que potencian o bloquean la transmisión en la unión neuromuscular
Fármacos que afectan a la unión neuromuscular por sus acciones similares a las de la acetilcolina, el bloqueo de la transmisión neuromuscular y la inactivación de la acetilcolina, el bloqueo de la transmisión neuromuscular y la inactivación de la acetilcolinesterasa.
Fármacos con acción similar a la acetilcolina. Muchos compuestos, por ejemplo la metacolina, el carbocol y la nicotina, tiene el mismo efecto sobre la fibra muscular que la acetilcolina. La diferencia entre estos fármacos y la acetilcolina consiste en que los fármacos no son destruidos por la colinesterasa, o son destruidos muy lentamente.
Fármacos que bloquean la transmisión en la unión neuromuscular
Un grupo de fármacos conocido como fármacos curariformes puede impedir el paso de los impulsos desde la terminación nerviosa hacia el musculo. Por ejemplo, la d-tubocurarina bloquea la acción de la acetilcolina sobre los receptores de acetilcolina de la fibra muscular, impidiendo así que aumente los suficientes la permeabilidad de los canales de la membrana muscular para iniciar un potencial de acción.
Fármacos que inactivan la acetilcolinesterasa. Tres fármacos particularmente bien conocidos inactivan la acetilcolinesterasa. En consecuencia, aumentan los niveles de acetilcolina con cada impulso nervioso sucesivo, provocando la acumulación de una gran cantidad de acetilcolina que estimula repetitivamente la fibra muscular. El efecto de la neostigmina y la fisostigmina puede durar varias horas. El fluorofosfato de diissopropilo, que es un potencial toxico gaseoso nervioso de uso militar, inactiva la acetilcolinesterasa durante semanas.
Miastenia grave que causa parálisis muscular
La parálisis muscular se produce por la incapacidad de las uniones neuromuscular para transmitir señales desde las fibras nerviosas a las fibras musculares. En cuanto a su patogenia, se piensa que la miastenia grave es una enfermedad autoinmunitaria en la que los pacientes han desarrollado anticuerpos que destruyen sus propios canales iónicos activados por la acetilcolina. Los potenciales que se observan en la terminación nerviosa de las fibras musculares son demasiados débiles para iniciar la apertura de los canales de sodio activados por el voltaje de modo que no se produce la despolarización de las fibras musculares. Si la enfermedad es lo suficientemente intensa, el paciente muere por parálisis, concretamente por parálisis de los músculos respiratorios. Sin embargo, la enfermedad puede mejorarse habitualmente mediante la administración de neostigmina o de cualquier otro fármaco anticolinesterasico, que permite que se acumulen cantidades de acetilcolina, que alcanzan niveles elevados en el espacio sináptico.
Potencial de acción muscular
La conducción de los potenciales de acción en las fibras nerviosas es cualitativamente similar, pero no cuantitativamente similar a la de las fibras musculares esqueléticas. Algunas de las diferencias y similitudes cuantitativas son las siguientes.
El potencial de membrana en reposo es aproximadamente de -80 a -90 mV en las fibras esqueléticas. Similar al de las fibras nerviosas mielinizadas grandes.
La duración del potencial de acción es de 1 a 5 ms en el musculo esquelético, aproximadamente cinco veces mayor que en los nervios mielinizados grandes.
La velocidad de conducción es de 3 a 5 m/s, aproximadamente 1/18 de la velocidad de conducción de las fibras nerviosas mielinizadas grandes que excitan al musculo esquelético.
Acoplamiento excitación – contracción
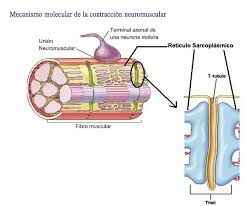
Los túbulos transversos son extensiones internas de la membrana celular. Los túbulos transversos siguen un trayecto transversal a las miofibrillas. Comienzan en la membrana celular y penetran desde un lado de la fibra muscular hasta el lado opuesto. En el punto en que los túbulos t se originan desde la membrana celular, están abiertos hacia el exterior y, por tanto, contienen líquido extracelular en su luz. Como los túbulos t son extensiones internas de la membrana celular, cuando un potencial de acción se propaga por la membrana de una fibra muscular, también se propaga a lo largo de los túbulos t hacia el interior de la fibra muscular. El retículo sarcoplasmatico está formado por túbulos longitudinales y cisternas terminales. Los túbulos longitudinales son paralelos a las miofibrillas y terminan en grandes cámaras denominadas cisternas terminales. Las cisternas terminales son contiguas a los túbulos t. En el musculo cardiaco, se localiza una red simple de túbulos t para cada sarcomero a la altura del disco Z. en el musculo esquelético de los mamíferos hay dos redes de túbulos t por cada sarcomero situado cerca de los dos extremos de los filamentos de miosina, que son los puntos en los que se crean las fuerzas mecánicas de la contracción muscular. Por tanto, el musculo esquelético de los mamíferos está organizado para lograr la excitación rápida de la contracción muscular.
Liberación de los iones calcio por las cisternas terminales del retículo sarcoplasmatico. Los iones calcio contenidos en retículo sarcoplasmatico son liberados cuando se produce un potencial de acción en los túbulos t adyacente. El potencial de acción parece provocar por sí mismo la apertura rápida de los canales de calcio a través de las membranas en las cisternas terminales del reticulosarcoplamatico. Estos canales permanecen abiertos durante el cual se liberan los iones calcio responsables de la contracción muscular hacia el sarcoplasma que rodea las miofibrillas.
La bomba de calcio retira los iones calcio del líquido sarcoplasmatico. Una bomba de calcio que actúa continuamente y que está localizada en las paredes de los túbulos longitudinales del retículo sarcoplasmatico bombea iones calcio desde las miofibrillas de nuevo hacia los túbulos sarcoplasmaticos. Esta bomba puede concentrar los inoes de calcio aproximadamente 10000 veces en el interior de los túbulos. Además en el interior del retículo hay una proteína denominada calsecuestrina, que puede proporcionar un aumento de hasta 40 veces más en el almacenamiento de calcio. Esta transferencia de calcio hacia el retículo sarcoplasmatico depleciona los iones calcio del líquido sarcoplasmatico, con lo que termina la contracción muscular.