Esta es tu primera entrada. Haz clic en el enlace Editar para modificarla o eliminarla, o bien crea una entrada nueva. Si quieres, usa esta entrada para explicar a los lectores por qué has empezado este blog y qué tienes previsto hacer con él.

Esta es tu primera entrada. Haz clic en el enlace Editar para modificarla o eliminarla, o bien crea una entrada nueva. Si quieres, usa esta entrada para explicar a los lectores por qué has empezado este blog y qué tienes previsto hacer con él.

El sistema urinario: anatomía funcional y formación de orina en los riñones.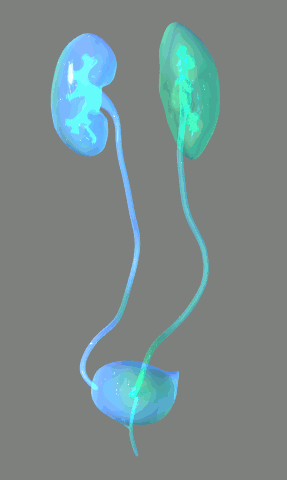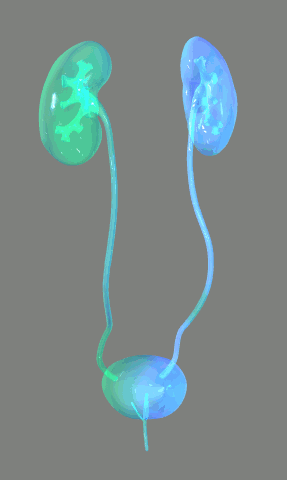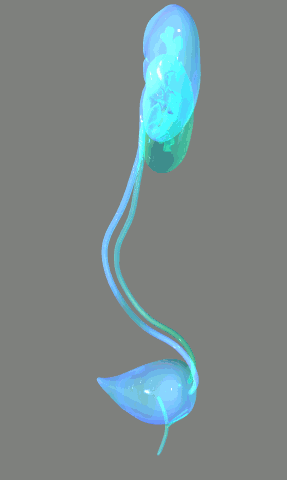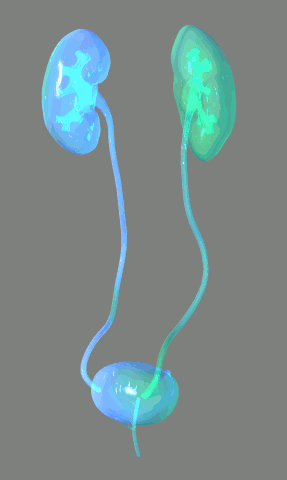 Los riñones realizan sus funciones más importantes filtrando el plasma y eliminando sustancias del filtrado con una intensidad variable, dependiendo de las necesidades del cuerpo. Finalmente, los riñones aclaran las sustancias no deseadas del filtrado excretándolas a la orina mientras devuelven las sustancias necesarias de nuevo a la sangre.
Los riñones realizan sus funciones más importantes filtrando el plasma y eliminando sustancias del filtrado con una intensidad variable, dependiendo de las necesidades del cuerpo. Finalmente, los riñones aclaran las sustancias no deseadas del filtrado excretándolas a la orina mientras devuelven las sustancias necesarias de nuevo a la sangre.
Los riñones ejercen numerosas funciones homeostáticas, entre ellas las siguientes:
Excreción de productos metabólicos de desecho y sustancias químicas extrañas.
Regulación de los equilibrios hídricos y electrolíticos.
Regulación de la osmolalidad del líquido corporal y de las concentraciones de electrólitos.
Regulación de la presión arterial. Regulación del equilibrio acido básico.
Regulación de la producción de eritrocitos. Secreción, metabolismo y excreción de hormonas. Gluconeogenia.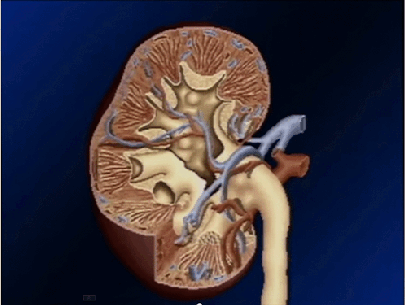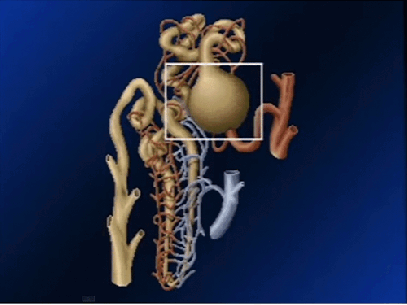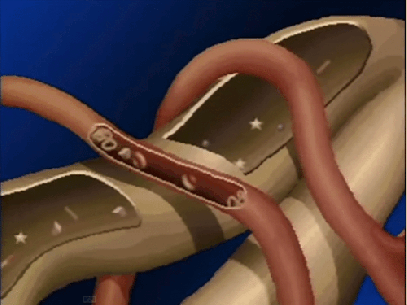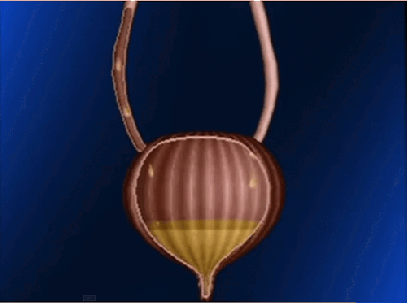 Excreción de productos metabólicos de desecho, sustancias químicas extrañas, fármacos y metabolitos de hormonas.
Excreción de productos metabólicos de desecho, sustancias químicas extrañas, fármacos y metabolitos de hormonas.
Los riñones son los principales medios de eliminación de los productos de desecho del metabolismo que ya no necesita el cuerpo. Estos productos son la urea (del metabolismo de los aminoácidos), la creatinina (de la creatina muscular), el ácido úrico (de los ácidos nucleicos), los productos finales del metabolismo de la hemoglobina (como la bilirrubina) y los metabolitos de varias hormonas.
Estos productos de desecho deben eliminarse del cuerpo tan rápidamente como se producen. Los riñones también eliminan la mayoría de las toxinas y otras sustancias extrañas que el cuerpo produce o ingiere, como los pesticidas, los fármacos y los aditivos alimentarios. Regulación del equilibrio hídrico y electrolítico
Regulación del equilibrio hídrico y electrolítico
Para el mantenimiento de la homeostasis, la excreción de agua y electrólitos debe corresponderse de forma precisa con su ingreso. Si los ingresos superan a la excreción, la cantidad de esa sustancia en el cuerpo aumentará. Si la ingestión es menor que la excreción, la cantidad de esa sustancia en el cuerpo se reducirá. Aunque pueden producirse desequilibrios transitorios (o cíclicos) de agua y electrólitos en diversas condiciones fisiológicas y fisiopatológicas asociadas con una entrada o excreción renal alteradas, el mantenimiento de la vida depende de la restauración del equilibrio de agua y electrólitos. En los 2 a 3 días siguientes del aumento de la ingestión de sodio, la excreción renal también aumenta hasta alrededor de 300 mEq/día, de manera que se restablece rápidamente el equilibrio entre la ingestión y la salida. Pero durante la adaptación renal en esos 2 a 3 días a la elevada ingestión de sodio se produce una acumulación modesta de sodio que incrementa ligeramente el volumen de líquido extracelular y desencadena cambios hormonales y otras respuestas compensadoras que indican a los riñones que aumenten la excreción de sodio.Regulación de la presión arterial
Los riñones desempeñan una función dominante en la regulación a largo plazo de la presión arterial al excretar cantidades variables de sodio y agua. Los riñones también contribuyen a la regulación a corto plazo de la presión arterial mediante la secreción de hormonas y factores o sustancias vasoactivos, como la renina, que dan lugar a la formación de productos vasoactivos.
Regulación del equilibrio acido-básico
Los riñones contribuyen a la regulación acido básico junto a los pulmones y los amortiguadores del líquido corporal mediante la excreción de ácidos y la regulación de los depósitos de amortiguadores en el líquido corporal. Los riñones son el único medio de eliminar ciertos tipos de ácidos, como el ácido sulfúrico y el ácido fosfórico, que genera el metabolismo de las proteínas.
Regulación de la producción de eritrocitos.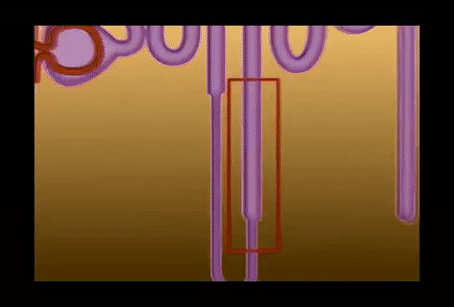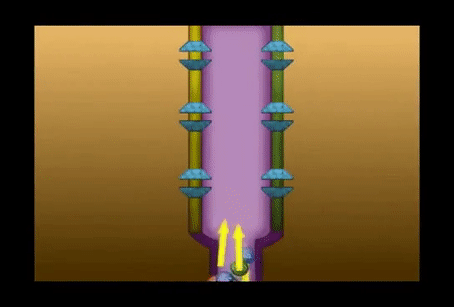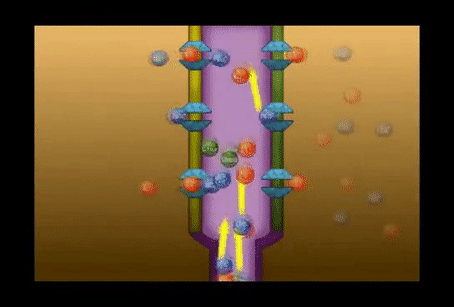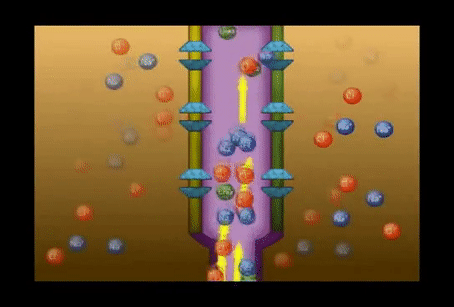 Los riñones secretan eritropoyetina, que estimula la producción de eritrocitos en las células madre hematopoyéticas de la médula ósea, un estímulo importante para la secreción de eritropoyetina por los riñones es la hipoxia. Los riñones son responsables normalmente de la mayor parte de la eritropoyetina secretada a la circulación. En las personas con una nefropatía grave o en las que se han extirpado los riñones y están en hemodiálisis, aparece una anemia grave debido a la menor producción de eritropoyetina.Regulación de la producción de 1,25-dihidroxivitamina D3
Los riñones secretan eritropoyetina, que estimula la producción de eritrocitos en las células madre hematopoyéticas de la médula ósea, un estímulo importante para la secreción de eritropoyetina por los riñones es la hipoxia. Los riñones son responsables normalmente de la mayor parte de la eritropoyetina secretada a la circulación. En las personas con una nefropatía grave o en las que se han extirpado los riñones y están en hemodiálisis, aparece una anemia grave debido a la menor producción de eritropoyetina.Regulación de la producción de 1,25-dihidroxivitamina D3
Los riñones producen la forma activa de la vitamina D, 1,25-dihidroxivitamina D3 (calcitriol), mediante la hidroxilación de esta vitamina en la posición número 1. El calcitriol es esencial para el depósito normal del calcio en el hueso y la reabsorción del calcio en el aparato digestivo, el calcitriol desempeña una función importante en la regulación del calcio y del potasio.Síntesis de glucosa
Los riñones sintetizan glucosa a partir de los aminoácidos y otros precursores durante el ayuno prolongado, un proceso denominado gluconeogenia. La capacidad de los riñones de añadir glucosa a la sangre durante períodos prolongados de ayuno rivaliza con la del hígado. En las nefropatías crónicas o en la insuficiencia renal aguda, estas funciones homeostáticas se interrumpen y aparecen con rapidez anomalías intensas en los volúmenes del líquido corporal y en su composición. Ante una insuficiencia renal completa se acumulan en el cuerpo suficiente potasio, ácidos, líquido y otras sustancias como para causar la muerte en unos días, a no ser que se inicien intervenciones clínicas como la hemodiálisis para restablecer, al menos parcialmente, los equilibrios de los líquidos y los electrólitos corporales.ANATOMIA FISIOLOGICA DE LOS RIÑONES
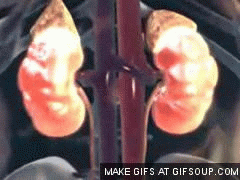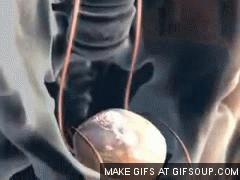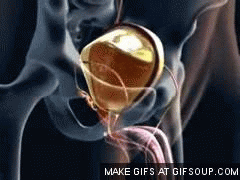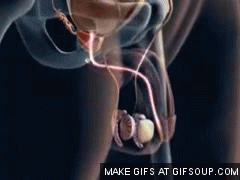
Los riñones se disponen en la pared posterior del abdomen, fuera de la cavidad peritoneal. Cada riñón de un ser humano adulto normal pesa unos 150 g y tiene el tamaño aproximado de un puño cerrado. La cara medial de cada riñón contiene una región con una muesca, llamada hilio, por la que pasan la arteria y vena renales, los linfáticos, la inervación y el uréter, que transporta la orina final desde el riñón hasta la vejiga, donde se almacena hasta que esta se vacía. El riñón está rodeado de una cápsula fibrosa y tensa que protege sus delicadas estructuras internas.
Si se cortan los riñones de arriba abajo, las dos regiones principales que pueden verse son la corteza externa y las regiones internas de la médula. La médula se divide en 8-10 masas de tejido en forma de cono llamadas pirámides renales. La base de cada pirámide se origina en el borde entre la corteza y la médula y termina en la papila, que se proyecta en el espacio de la pelvis renal, una continuación en forma de abanico de la porción superior del uréter.
El borde externo de la pelvis se divide en bolsas abiertas, llamadas cálices mayores, que se extienden hacia abajo y se dividen en los cálices menores, que recogen la orina de los túbulos de cada papila. Las paredes de los cálices, la pelvis y el uréter contienen elementos contráctiles que empujan la orina hacia la vejiga, donde se almacena hasta que se vacía en la micción.
Irrigación renal
El riego sanguíneo de los dos riñones es normalmente de alrededor del 22% del gasto cardíaco, o 1.100 ml/min. La arteria renal entra en el riñón a través del hilio y después se ramifica progresivamente hasta formar las arterias interlobulares, las arterias arciformes, las arterias interlobulillares (también denominadas arterias radiales) y las arteriolas aferentes, que acaban en los capilares glomerulares, donde se filtran grandes cantidades de líquido y solutos (excepto las proteínas plasmáticas) para comenzar la formación de orina. Los extremos distales de los capilares de cada glomérulo coalescen hasta formar la arteriola eferente, que llega a la segunda red capilar, los capilares peritubulares, que rodean a los túbulos renales.La circulación renal tiene la particularidad de contar con dos lechos capilares, los capilares glomerulares y los peritubulares, que están dispuestos en serie y están separados por las arteriolas eferentes. Estas arteriolas ayudan a regular la presión hidrostática en los dos grupos de capilares. La presión hidrostática alta en los capilares glomerulares (de unos 60 mmHg) da lugar a una filtración rápida, mientras que una presión hidrostática mucho menor en los capilares peritubulares (de unos 13 mmHg) permite una reabsorción rápida de líquido.
Al ajustar la resistencia de las arteriolas aferente y eferente, los riñones pueden regular la presión hidrostática en los capilares glomerulares y peritubulares, cambiando la filtración glomerular, la reabsorción tubular o ambas en respuesta a las demandas homeostáticas del cuerpo. Los capilares peritubulares se vacían en los vasos del sistema venoso, que discurren paralelos a los vasos arteriolares. Los vasos sanguíneos del sistema venoso forman progresivamente la vena interlobulillar, la vena arciforme, la vena interlobular y la vena renal, que abandona el riñón junto a la arteria renal y el uréter.NEFRONA COMO UNIDAD FUNCIONAL DEL RIÑON
Cada riñón humano contiene alrededor de 800.000 a 1.000.000 de nefronas, cada una de las cuales es capaz de formar orina. El riñón no puede regenerar nefronas nuevas. Por tanto, en la lesión, la enfermedad o el envejecimiento renal normal, el número de nefronas se reduce gradualmente.
Cada nefrona contiene:
Un penacho de capilares glomerulares llamado glomérulo, por el que se filtran grandes cantidades de líquido desde la sangre.
Un túbulo largo en el que el líquido filtrado se convierte en orina en su camino a la pelvis del riñón.
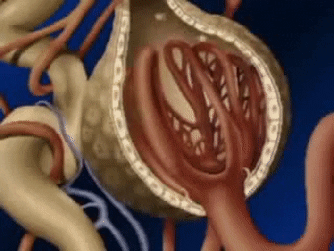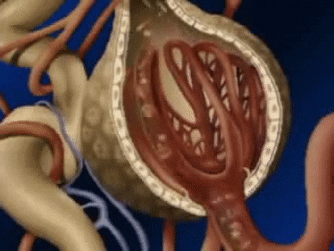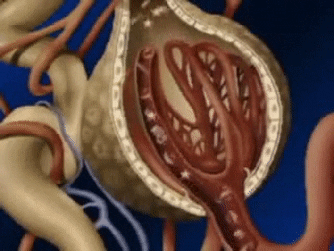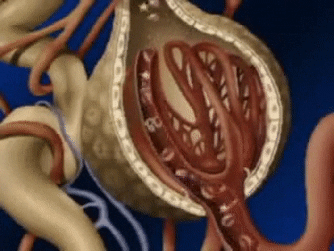
El glomérulo contiene una red de capilares glomerulares que se ramifican y anastomosan y que, comparados con otros capilares, tienen una presión hidrostática alta (de unos 60 mmHg).
Los capilares glomerulares están revestidos de células epiteliales y todo el glomérulo está cubierto por la cápsula de Bowman.
El líquido filtrado desde los capilares glomerulares circula hacia la cápsula de Bowman y después al túbulo proximal, que se encuentra en la corteza del riñón. Desde el túbulo proximal, el líquido fluye hacia el asa de Henle, que desciende hasta la médula renal. Cada asa consta de una rama descendente y otra ascendente.
Las paredes de la rama descendente y el segmento inferior de la rama ascendente son muy finas y de ahí que se denominen segmento fino del asa de Henle. Después de que la rama ascendente del asa ha vuelto a la corteza, su pared se engruesa mucho y se denomina segmento grueso del asa ascendente. Al final de la rama ascendente gruesa hay un segmento corto, que tiene en su pared una placa de células epiteliales especializadas conocida como mácula densa.
Más allá de la mácula densa el líquido entra en el túbulo distal, que, como el túbulo proximal, se dispone en la corteza renal. Al túbulo distal le siguen el túbulo conector y el túbulo colector cortical, que conduce al conducto colector cortical.
Las partes iniciales de 8 a 10 conductos colectores corticales se unen para formar un solo conducto colector mayor que discurre hacia abajo al interior de la médula y se convierte en el conducto colector medular. Los conductos colectores se funden para formar progresivamente conductos cada vez mayores que finalmente se vacían en la pelvis renal a través de las puntas de las papilas renales. En cada riñón hay unos 250 conductos colectores muy grandes y cada uno recoge la orina de unas 4.000 nefronas.Diferencias regionales en la estructura de la nefrona: nefronas corticales y yuxtamedulares.Las nefronas que tienen glomérulos localizados en la corteza externa se denominan nefronas corticales; tienen asas de Henle cortas que penetran solo una distancia corta en la médula. Alrededor del 20-30% de las nefronas tienen glomérulos que se disponen en la profundidad de la corteza renal cerca de la médula y se denominan nefronas yuxtamedulares.
Estas nefronas tienen asas de Henle grandes que discurren hasta la médula, en algunos casos con un recorrido completamente intramedular hasta desembocar en las papilas renales. Las estructuras vasculares que irrigan las nefronas yuxtamedulares también difieren de las que irrigan las nefronas corticales. En las nefronas corticales todo el sistema tubular está rodeado de una red extensa de capilares peritubulares.
En las nefronas yuxtamedulares, las arteriolas eferentes largas se extienden desde los glomérulos hasta la médula externa y después se dividen en capilares peritubulares especializados, llamados vasos rectos, que se extienden hasta la médula al lado de las asas de Henle. Como las asas de Henle, los vasos rectos vuelven a la corteza y se vacían en las venas corticales. Esta red especializada de capilares en la médula desempeña una función esencial en la formación de una orina concentrada.Micción
La micción es el proceso mediante el cual la vejiga urinaria se vacía cuando está llena. Este proceso se realiza en dos pasos. Primero, la vejiga se llena progresivamente hasta que la tensión en sus paredes aumenta por encima de un umbral.
Esta tensión desencadena el segundo paso, que es un reflejo nervioso, llamado reflejo miccional, que vacía la vejiga o, si esto falla, provoca al menos un deseo de orinar. Aunque el reflejo miccional es un reflejo medular autónomo, centros presentes en la corteza cerebral o en el tronco del encéfalo pueden inhibirlo o facilitarlo. Anatomía fisiológica de la vejiga La vejiga urinaria, es una cámara de músculo liso compuesta de dos partes principales:
El cuerpo, que es la principal parte de la vejiga en la que se acumula la orina.
El cuello, que es una extensión en forma de abanico del cuerpo, que pasa en sentido inferior y anterior hasta el triángulo urogenital y se conecta con la uretra. La parte inferior del cuello de la vejiga también se llama uretra posterior por su relación con la uretra.El músculo liso de la vejiga se llama músculo detrusor. Sus fibras musculares se extienden en todas las direcciones y, cuando se contraen, pueden aumentar la presión en la vejiga hasta 40-60 mmHg. Luego la contracción del músculo detrusor es un paso importante en el vaciamiento de la vejiga. Las células musculares lisas del músculo detrusor se fusionan entre sí de manera que existen vías eléctricas de baja resistencia de una célula muscular a otra.
De este modo un potencial de acción puede propagarse a través del músculo detrusor, desde una célula muscular a la siguiente, para provocar la contracción de toda la vejiga a la vez.En la pared posterior de la vejiga, inmediatamente por encima del cuello de la vejiga, hay una pequeña zona triangular llamada trígono. En la parte más inferior del vértice del trígono, el cuello de la vejiga se abre en la uretra posterior, y los dos uréteres entran en la vejiga en los ángulos más superiores del trígono. El trígono puede identificarse por el hecho de que su mucosa, el recubrimiento interno de la vejiga, es lisa, al contrario que el resto de la mucosa vesical, que está plegada y forma arrugas.
Cada uréter, en su entrada en la vejiga, discurre en sentido oblicuo a través del músculo detrusor y después pasa otros 1-2 cm por debajo de la mucosa vesical antes de vaciarse en la vejiga. El cuello de la vejiga (uretra posterior) tiene 2 a 3 cm de longitud, y su pared está compuesta del músculo detrusor entrelazado con una gran cantidad de tejido elástico. El músculo en esta zona se llama esfínter interno. Su tono natural mantiene normalmente el cuello de la vejiga y la uretra posterior vacías de orina y, por tanto, impide el vaciamiento de la vejiga hasta que la presión en la parte principal de la vejiga aumenta por encima de un umbral crítico.
Más allá de la uretra posterior, la uretra atraviesa el diafragma urogenital, que contiene una capa de músculo llamada esfínter externo de la vejiga. Este músculo es un músculo esquelético voluntario, al contrario que el músculo del cuerpo de la vejiga y del cuello de la vejiga, que es totalmente músculo liso. El músculo del esfínter externo está bajo un control voluntario del sistema nervioso y puede usarse para impedir conscientemente la micción incluso cuando los controles involuntarios intentan vaciar la vejiga.Inervación de la vejiga
La principal inervación nerviosa de la vejiga es a través de los nervios pélvicos, que conectan con la médula espinal a través del plexo sacro, sobre todo los segmentos S2 y S3. (En los nervios pélvicos discurren fibras nerviosas sensitivas y motoras. Las fibras sensitivas detectan el grado de distensión de la pared de la vejiga. Las señales de distensión de la uretra posterior son especialmente fuertes y son responsables sobre todo de iniciar los reflejos que provocan el vaciado de la vejiga.Los nervios motores transmitidos en los nervios pélvicos son fibras parasimpáticas. Estas fibras terminan en las células ganglionares localizadas en la pared de la vejiga. Después, nervios posganglionares cortos inervan el músculo detrusor. Además de los nervios pélvicos, otros dos tipos de inervación son importantes para la función vesical.
Los más importantes son las fibras motoras esqueléticas que llegan a través del nervio pudendo hasta el esfínter vesical externo. Se trata de fibras nerviosas somáticas que inervan y controlan el músculo esquelético voluntario del esfínter. Además, la vejiga recibe la inervación simpática de la cadena simpática a través de los nervios hipogástricos, que conectan sobre todo con el segmento L2 de la médula espinal. Estas fibras simpáticas estimulan principalmente los vasos sanguíneos y tienen poco que ver con la contracción de la vejiga. Algunas fibras nerviosas sensitivas también pasan a través de los nervios simpáticos y pueden ser importantes en la sensación de plenitud y, en algunos pacientes, de dolor.Transporte de orina desde el riñón hasta los uréteres y la vejiga
La orina que sale de la vejiga tiene prácticamente la misma composición que el líquido que fluye de los conductos colectores; no hay cambios significativos en la composición de la orina en su camino a través de los cálices renales hasta los uréteres y la vejiga.
La orina que fluye desde los conductos colectores hacia los cálices renales estira los cálices e incrementa su actividad de marcapasos intrínseca, lo que a su vez inicia las contracciones peristálticas que se propagan a la pelvis renal y después a lo largo de la longitud del uréter, forzando así la orina desde la pelvis renal hacia la vejiga. En los adultos, los uréteres tienen normalmente de 25 a 35 cm de longitud.Las paredes de los uréteres contienen músculo liso y están inervadas por nervios simpáticos y parasimpáticos, así como por un plexo intramural de neuronas y fibras nerviosas que se extiende a lo largo de toda la longitud de los uréteres. Igual que sucede con otros músculos lisos viscerales, las contracciones peristálticas en el uréter se potencian con la estimulación parasimpática y se inhiben con la estimulación simpática.
Los uréteres entran en la vejiga a través del músculo detrusor en la región del trígono vesical. Los uréteres discurren normalmente en sentido oblicuo durante varios centímetros a través de la pared vesical. El tono normal del músculo detrusor en la pared de la vejiga tiende a comprimir el uréter, lo que impide el retroceso (reflujo) de orina desde la vejiga cuando la presión aumenta en ella durante la micción o la compresión de la vejiga.Cada onda peristáltica a lo largo del uréter aumenta la presión dentro del uréter de manera que la región que atraviesa la pared de la vejiga se abre y permite que la orina fluya hacia la vejiga. En algunas personas, la distancia que el uréter discurre a través de la pared vesical es menor de lo normal, de manera que la contracción de la vejiga durante la micción no siempre ocluye completamente el uréter. Como resultado, parte de la orina de la vejiga se impulsa hacia atrás, hasta los uréteres, un trastorno que se conoce como reflujo vesicoureteral. Este reflujo puede aumentar el tamaño de los uréteres y, si es intenso, incrementar la presión en los cálices y las estructuras renales de la médula, provocando lesiones en estas regiones.Sensación de dolor en los uréteres y reflejo ureterorrenal
Los uréteres reciben una buena inervación de fibras nerviosas del dolor. Cuando un uréter se bloquea (p. ej., por un cálculo ureteral), se produce una constricción refleja intensa acompañada de un dolor intenso. Además, los impulsos dolorosos provocan un reflejo simpático hacia el riñón que contrae las arteriolas renales, lo que reduce la producción renal de orina. Este efecto se llama reflejo ureterorrenal y es importante para evitar un flujo excesivo de líquido hacia la pelvis de un riñón con un uréter obstruido.Reflejo miccional
Las señales sensitivas de los receptores de distensión vesicales son conducidas a los segmentos sacros de la médula a través de los nervios pélvicos, y después vuelven de nuevo a la vejiga a través de las fibras nerviosas parasimpáticas de estos mismos nervios. Cuando la vejiga está solo parcialmente llena, estas contracciones miccionales suelen relajarse espontáneamente tras una fracción de minuto, el músculo detrusor deja de contraerse y la presión vuelve a su valor basal. A medida que la vejiga continúa llenándose, los reflejos miccionales se hacen más frecuentes y provocan contracciones mayores del músculo detrusor. Una vez que comienza el reflejo miccional, este es «autorregenerativo».Es decir, que la contracción inicial de la vejiga activa los receptores de distensión que causan un mayor incremento en los impulsos sensitivos que van desde la vejiga y la uretra posterior, lo que aumenta más la contracción refleja de la vejiga; después el ciclo se repite una y otra vez hasta que la vejiga alcanza un alto grado de contracción. Después de algunos segundos a más de 1 min, el reflejo autorregenerativo comienza a agotarse y el ciclo regenerativo del reflejo miccional cesa, lo que permite la relajación de la vejiga.
De este modo el reflejo miccional es un solo ciclo completo de:
Aumento rápido y progresivo de la presión.
Un período de presión mantenida.
Un retorno de la presión al tono basal de la vejiga.
Una vez que se ha producido el reflejo miccional pero no se ha vaciado la vejiga, los elementos nerviosos de este reflejo suelen permanecer en un estado de inhibición durante unos minutos a 1 h o más debido a que aparece otro reflejo miccional.
A medida que la vejiga se llena más y más, los reflejos miccionales son más y más frecuentes y poderosos. Una vez que el reflejo miccional es lo suficientemente poderoso, provoca otro reflejo, que pasa a través de los nervios pudendos hasta el esfínter externo para inhibirlo. Si esta inhibición es más potente en el encéfalo que las señales constrictoras voluntarias al esfínter externo, se produce la micción. Si no, la micción no se produce hasta que la vejiga se llena más y el reflejo miccional se hace más potente.Facilitación o inhibición de la micción por el encéfalo
El reflejo miccional es un reflejo medular autónomo, pero centros encefálicos pueden inhibirlo o facilitarlo.
Estos centros son:
Centros facilitadores e inhibidores potentes situados en el tronco del encéfalo, sobre todo en la protuberancia.
Varios centros localizados en la corteza cerebral que son sobre todo inhibidores, pero pueden hacerse excitadores. El reflejo miccional es la causa básica de la micción, pero los centros superiores ejercen normalmente un control final sobre la micción como sigue:1. Los centros superiores mantienen el reflejo miccional parcialmente inhibido, excepto cuando se desea la micción.
2. Los centros superiores pueden impedir la micción, incluso aunque se produzca el reflejo miccional, mediante una contracción tónica del esfínter vesical externo hasta que se presente un momento adecuado.
3. Cuando es el momento de la micción, los centros corticales pueden facilitar que los centros de la micción sacros ayuden a iniciar el reflejo miccional y al mismo tiempo inhibir el esfínter urinario externo para que la micción pueda tener lugar.
La micción voluntaria suele iniciarse de la siguiente forma. En primer lugar, una persona contrae voluntariamente los músculos abdominales, lo que aumenta la presión en la vejiga y permite la entrada de una cantidad extra de orina en el cuello de la vejiga y en la uretra posterior bajo presión, lo que estira sus paredes. Esta acción estimula los receptores de distensión, lo que excita el reflejo miccional y a la vez inhibe el esfínter uretral externo. Habitualmente se vaciará toda la orina dejando raramente más de 5-10 ml en la vejiga.La formación de orina es resultado de la filtración glomerular, la reabsorción tubular y la secreción tubular.
La formación de orina comienza cuando una gran cantidad de líquido que casi no dispone de proteínas se filtra desde los capilares glomerulares a la cápsula de Bowman.
La mayoría de las sustancias del plasma, excepto las proteínas, se filtran libremente, de manera que su concentración en el filtrado glomerular de la cápsula de Bowman es casi la misma que en el plasma. A medida que el líquido abandona la cápsula de Bowman y pasa a través de los túbulos, se modifica por la reabsorción de agua y solutos específicos de nuevo hacia la sangre o por la secreción de otras sustancias desde los capilares peritubulares hacia los túbulos.Filtración, reabsorción y secreción de diferentes sustancias
En general, la reabsorción tubular es cuantitativamente más importante que la secreción tubular en la formación de la orina, pero la secreción es importante para determinar las cantidades de iones potasio e hidrógeno y algunas otras sustancias que se excretan por la orina. La mayoría de las sustancias que deben eliminarse de la sangre, en especial los productos finales del metabolismo, como la urea, la creatinina, el ácido úrico y los uratos, se reabsorben mal y por ello se excretan en grandes cantidades en la orina.
Ciertas sustancias extrañas y fármacos se reabsorben mal pero, además, se secretan desde la sangre a los túbulos, de manera que su excreción es alta. Por el contrario, los electrólitos, como los iones cloro, sodio y bicarbonato, se reabsorben mucho, de manera que solo se detectan en la orina pequeñas cantidades. Ciertas sustancias nutritivas, como los aminoácidos y la glucosa, se reabsorben completamente de los túbulos y no aparecen en la orina, aunque los capilares glomerulares filtren grandes cantidades.Cada uno de los procesos (filtración glomerular, reabsorción y secreción tubular) está regulado de acuerdo con las necesidades del cuerpo. Por ejemplo, cuando hay un exceso de sodio en el cuerpo, la intensidad con la que el sodio se filtra normalmente aumenta y se reabsorbe una fracción menor del sodio filtrado, lo que da lugar a una mayor excreción en la orina.
Para la mayoría de las sustancias, la filtración y la reabsorción son muy intensas comparadas con la excreción. Por tanto, incluso cambios ligeros en la filtración o la reabsorción pueden dar lugar a cambios grandes en la excreción renal. Por ejemplo, un aumento de la filtración glomerular (FG) de solo un 10% (de 180 a 198 l/día) aumentaría el volumen de orina 13 veces (de 1,5 a 19,5 l/día) si la reabsorción tubular permaneciera constante. En realidad, los cambios en la filtración glomerular y en la reabsorción tubular suelen actuar de manera coordinada para producir los cambios necesarios en la excreción renal.Brandon nazario vazquez balanzar 1-B
La ingestión y la pérdida de líquido están equilibradas durante las situaciones estables
Resulta llamativa la relativa constancia de los líquidos corporales ya que hay un intercambio continuo de líquido y solutos con el ambiente externo, así como dentro de los diferentes compartimientos del cuerpo.
El agua ingresa en el cuerpo a través de dos fuentes principales: se ingiere en forma de líquidos o de agua de los alimentos, que juntos suponen alrededor de 2.100 ml/día de líquidos corporales. Se sintetiza en el cuerpo por la oxidación de los hidratos de carbono, en una cantidad de unos 200 ml/día.
Estos mecanismos proporcionan un ingreso total de agua de unos 2.300 ml/día.
Perdida diaria de agua corporal, Pérdida insensible de agua
Parte de las pérdidas de agua no puede regularse de manera precisa. Por ejemplo, los seres humanos experimentan una pérdida continua de agua por evaporación de las vías aéreas y por difusión a través de la piel, y en conjunto son responsables de alrededor de 700 ml/día de pérdida de agua en condiciones normales. A esto se le denomina pérdida insensible de agua porque no somos conscientes de ella, aunque se produzca continuamente en todos los seres humanos vivos.
La pérdida media de agua por difusión a través de la piel es de unos 300-400 ml/día. Esta pérdida la minimiza la capa cornificada llena de colesterol de la piel, que constituye una barrera contra la pérdida excesiva por difusión. La pérdida insensible de agua a través de la vía aérea es de unos 300-400 ml/día. A medida que el aire entra en la vía aérea, se satura de humedad hasta una presión de agua de unos 47 mmHg hasta que se espira. Pérdida de líquido en el sudor y heces
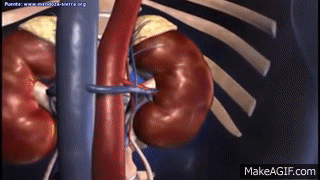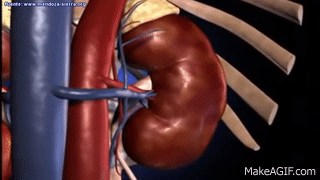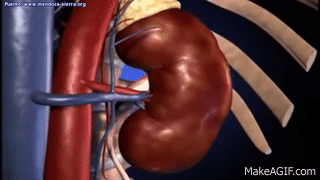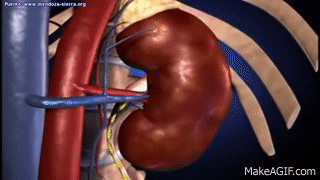
La cantidad de agua perdida por el sudor es muy variable dependiendo de la actividad física y de la temperatura ambiental. El volumen de sudor es normalmente de unos 100 ml/día, pero en un clima muy cálido o durante el ejercicio intenso, la pérdida de líquidos en el sudor aumenta en ocasiones a 1-2 l/h. Esta pérdida vaciaría rápidamente los líquidos corporales si la ingestión no aumentara mediante la activación del mecanismo de la sed. Solo se pierde normalmente una pequeña cantidad de agua (100 ml/día) en las heces. Esta pérdida puede aumentar a varios litros al día en personas con diarrea intensa. Por esta razón la diarrea intensa puede poner en peligro la vida si no se corrige en unos días.
Pérdida de agua por los riñones
El medio más importante por el que el cuerpo mantiene un equilibrio entre los ingresos y las pérdidas, así como el equilibrio entre el ingreso y la salida de la mayoría de los electrólitos en el cuerpo, es controlando la intensidad con la que los riñones excretan estas sustancias. Por ejemplo, el volumen de orina puede ser tan solo de 0,5 l/día en una persona deshidratada o tan alta como de 20 l/día en una persona que ha bebido cantidades enormes de agua.
Compartimientos del líquido corporal
El líquido corporal total se distribuye sobre todo entre dos compartimientos: el líquido extracelular y el líquido intracelular. El líquido extracelular se divide en el líquido intersticial y el plasma sanguíneo.
Existe otro pequeño compartimiento de líquido que se denomina líquido transcelular. Este compartimiento comprende el líquido de los espacios sinovial, peritoneal, pericárdico e intracelular, así como el líquido cefalorraquídeo. Constituyen alrededor de 1 a 2 l.
Compartimiento del líquido intracelular
Unos 28 de los 42 l de líquido corporal están contenidos de los 100 billones de células y se les denomina en conjunto líquido intracelular. Por tanto, el líquido intracelular constituye alrededor del 40% del peso corporal total en una persona «media».
Compartimiento del líquido extracelular
Todos los líquidos del exterior de las células se denominan en conjunto líquido extracelular y constituyen alrededor del 20% del peso corporal, o unos 14 l en un hombre adulto de 70 kg. Los dos compartimientos más grandes del líquido extracelular son el líquido intersticial, que supone hasta más de tres cuartas partes (11 l) del líquido extracelular, y el plasma, que supone casi una cuarta parte del líquido extracelular o unos 3 l. El plasma es la parte no celular de la sangre; intercambia sustancias continuamente con el líquido intersticial a través de poros de las membranas capilares.
Volumen sanguíneo
La sangre contiene líquido extracelular (el líquido del plasma) y líquido intracelular (el líquido de los eritrocitos). Sin embargo, la sangre se considera un compartimiento líquido separado porque está contenida en su propia cámara, el aparato circulatorio.
Hematocrito
El hematocrito es la fracción de la sangre compuesta de eritrocitos, lo que se determina centrifugando la sangre en un «tubo de hematocrito» hasta que todas las células se acumulan en el fondo. Dado que el centrifugado no compacta completamente los eritrocitos, alrededor de un 3-4% del plasma permanecen atrapado entre las células, y el hematocrito verdadero es solo de alrededor de un 96% del hematocrito medido. En los hombres, el hematocrito medido es normalmente de alrededor de 0,4 y en las mujeres, de alrededor de 0,36. En personas con anemia grave, el hematocrito puede reducirse hasta tan solo 0,1, un valor apenas suficiente para sustentar la vida. Por el contrario, en aquellas personas con trastornos en los que hay una producción excesiva de eritrocitos se produce una policitemia. En estas personas, el hematocrito puede aumentar a 0,65.
Constituyentes de los líquidos extracelular e intracelular
La composición iónica del plasma y del líquido intersticial es similar
Debido a que el plasma y el líquido intersticial están separados solo por membranas capilares muy permeables, su composición iónica es similar. La diferencia más importante entre estos dos compartimientos es la mayor concentración de proteínas en el plasma; debido a que los capilares tienen una permeabilidad baja a las proteínas plasmáticas, solo pequeñas cantidades de proteínas pasan a los espacios intersticiales en la mayoría de los tejidos.
Debido al efecto Donnan, la concentración de iones con carga positiva (cationes) es ligeramente superior en el plasma (alrededor de un 2%) que en el líquido intersticial. Las proteínas plasmáticas tienen una carga negativa neta y por ello tienden a ligar cationes, como iones sodio o potasio, manteniendo cantidades extra de estos cationes en el plasma junto a las proteínas plasmáticas. Por el contrario, los iones con carga negativa (aniones) tienden a tener una concentración ligeramente superior en el líquido intersticial que en el plasma, porque las cargas negativas de las proteínas plasmáticas repelen los aniones con carga negativa. Pero, con un sentido práctico, las concentraciones de iones en el líquido intersticial y en el plasma se consideran aproximadamente iguales.
Constituyentes del líquido intracelular
El líquido intracelular está separado del líquido extracelular por una membrana celular que es muy permeable al agua, pero no a la mayoría de los electrólitos del cuerpo. Las células contienen grandes cantidades de proteínas, casi cuatro veces más que en el plasma.
Medida de los volúmenes de líquido en los diferentes compartimientos hídricos del cuerpo: el principio de la dilución del indicador
El método de «dilución del indicador» de medida del volumen de un compartimiento líquido, se basa en el principio de la conservación de la masa, lo que significa que la masa total de una sustancia tras la dispersión en el compartimiento líquido será la misma que la masa total inyectada en el compartimiento.
Si ninguna de las sustancias sale del compartimiento, la masa total de la sustancia en el compartimiento (volumen B × concentración B) será igual a la masa total de la sustancia inyectada (volumen A × concentración A). Mediante un simple reordenamiento de la ecuación, podemos calcular el volumen desconocido de la cámara B como:
La composición iónica del plasma y del líquido intersticial es similar
Debido a que el plasma y el líquido intersticial están separados solo por membranas capilares muy permeables, su composición iónica es similar.
La diferencia más importante entre estos dos compartimientos es la mayor concentración de proteínas en el plasma; debido a que los capilares tienen una permeabilidad baja a las proteínas plasmáticas, solo pequeñas cantidades de proteínas pasan a los espacios intersticiales en la mayoría de los tejidos.
Constituyentes del líquido intracelular
El líquido intracelular está separado del líquido extracelular por una membrana celular que es muy permeable al agua, pero no a la mayoría de los electrólitos del cuerpo. Al contrario que el líquido extracelular, el líquido intracelular contiene solo mínimas cantidades de iones sodio y cloro y casi ningún ion calcio.
En cambio, contiene grandes cantidades de iones potasio y fosfato más cantidades moderadas de iones magnesio y sulfato, todos los cuales están en concentraciones bajas en el líquido extracelular.
Osmolalidad y osmolaridad La concentración osmolal de una solución se denomina osmolalidad cuando la concentración se expresa en osmoles por kilogramo de agua; se llama osmolaridad cuando se expresa en osmoles por litro de solución.
En soluciones diluidas, como los líquidos corporales, estos dos términos pueden usarse casi de forma sinónima porque las diferencias son pequeñas.
En la mayoría de los casos es más fácil expresar las cantidades de líquido corporal en litros de líquido en lugar de hacerlo en kilogramos de agua.
La mayoría de los cálculos usados en la clínica y los cálculos expresados en los siguientes capítulos se basan en osmolaridades en lugar de en osmolalidades
Líquidos isotónicos, hipotónicos e hipertónicos
Se dice que este tipo de solución es isotónica porque ni encoge ni hincha las células. Ejemplos de soluciones isotónicas son la solución de cloruro de sodio al 0,9% o la solución de glucosa al 5%. Estas soluciones son importantes en la medicina clínica porque pueden infundirse en la sangre sin poner en peligro el equilibrio osmótico entre los líquidos intracelular y extracelular Líquidos isoosmóticos, hiperosmóticos e hipoosmóticos Los términos isotónico, hipotónico e hipertónico se refieren a si las soluciones provocarán un cambio en el volumen celular.
La tonicidad de la solución depende de la concentración de los solutos no difusibles. Sin embargo, algunos solutos pueden atravesar la membrana celular. Las soluciones que poseen una osmolaridad igual a la de la célula se llaman isoosmóticas, sin importar si el soluto puede o no atravesar la membrana celular. Los términos hiperosmótico e hipoosmótico se refieren a soluciones que tienen una osmolaridad mayor o inferior, respectivamente, que el líquido extracelular normal, sin importar si el soluto puede o no atravesar la membrana celular.
Las sustancias que atraviesan fácilmente las membranas, como la urea, pueden causar desplazamientos transitorios del volumen líquido entre los líquidos intracelular y extracelular, pero con suficiente tiempo, las concentraciones de estas sustancias se igualarán en los dos compartimientos y ejercerán un escaso efecto sobre el volumen intracelular en condiciones estables.
El equilibrio osmótico entre los líquidos intracelular y extracelular se alcanza con rapidez
La transferencia de líquido a través de la membrana celular es tan rápida que cualquier diferencia en la osmolaridad entre los dos compartimientos se corrige en segundos o, como mucho, en minutos. Este movimiento rápido de agua a través de la membrana celular no significa que se produzca un equilibrio completo entre los compartimientos extracelular e intracelular en todo el cuerpo en un período corto. La razón es que el líquido suele entrar en el cuerpo a través del intestino y debe transportarse a través de la sangre a todos los tejidos antes de completar el equilibrio osmótico. Suelen tardarse unos 30 min en conseguir el equilibrio osmótico en todo el cuerpo tras beber agua. Volumen y osmolalidad de los líquidos intracelular y extracelular en estados anormales
Algunos de los factores que pueden hacer que los volúmenes extracelular e intracelular cambien son el exceso de ingestión o de retención renal de agua, la deshidratación, la infusión intravenosa de diferentes tipos de soluciones, la pérdida de grandes cantidades de líquido por el aparato digestivo y la pérdida de cantidades anormales de líquido a través del sudor o de los riñones. Pueden calcularse los cambios en los volúmenes de líquido extracelular e intracelular y los tipos de tratamiento que deben instaurarse teniendo en cuenta los principios básicos:
1. El agua se mueve rápidamente a través de las membranas celulares; por tanto, las osmolaridades de los líquidos intracelular y extracelular permanecen casi exactamente iguales excepto durante unos minutos después de un cambio en uno de los compartimientos.
2. Las membranas celulares son casi completamente impermeables a muchos solutos, como el sodio y el cloruro; por tanto, el número de osmoles en el líquido extracelular e intracelular permanece generalmente constante a no ser que se añadan o se retiren solutos en el compartimiento extracelular. Hiponatremia e Hipernatremia La osmolaridad plasmática no se mide habitualmente, pero como el sodio y sus aniones asociados (sobre todo el cloro) son responsables de más del 90% del soluto en el líquido extracelular, la concentración plasmática de sodio es un indicador razonable de la osmolaridad plasmática en muchas condiciones.
Cuando la concentración plasmática de sodio se reduce más de unos pocos miliequivalentes por debajo de la normalidad (unos 142 mEq/l), se dice que una persona tiene hiponatremia. Cuando la concentración plasmática de sodio está elevada por encima de lo normal, se dice que una persona tiene hipernatremia Causas de hiponatremia: exceso de agua o pérdida de sodio La reducción de la concentración plasmática de sodio puede deberse a una pérdida de cloruro de sodio en el líquido extracelular o a una adición de un exceso de agua al líquido extracelular.
Una pérdida primaria de cloruro de sodio suele dar lugar a una hiponatremia-deshidratación y se acompaña de una reducción del volumen de líquido extracelular. Los trastornos que pueden causar una hiponatremia debida a la pérdida de cloruro de sodio son la diarrea y los vómitos.
El consumo excesivo de diuréticos que inhiben la capacidad de los riñones de conservar el sodio y ciertos tipos de nefropatías que cursan con pérdida de sodio pueden provocar también grados leves de hiponatremia.
Consecuencias de la hiponatremia: inflamación celular Los rápidos cambios en el volumen celular como consecuencia de la hiponatremia pueden tener efectos profundos en la función de los tejidos y los órganos, especialmente el encéfalo. Una rápida reducción en la concentración de sodio en plasma puede provocar un edema de las células encefálicas y síntomas neurológicos, como cefalea, náuseas, letargo y desorientación. Si la concentración de sodio en plasma disminuye rápidamente por debajo de 115-120 mmol/l, la inflamación encefálica puede conducir a convulsiones, coma, daño cerebral permanente y muerte.
Consecuencias de la hipernatremia: contracción celular La hipernatremia es mucho menos común que la hiponatremia y los síntomas graves suelen producirse únicamente con aumentos rápidos e importantes en la concentración de sodio en plasma de más de 158-160 mmol/l.
Un motivo que explica este fenómeno es que la hipernatremia promueve una sed intensa y estimula la secreción de hormona antidiurética, que protege contra un aumento importante en el sodio en el plasma y el líquido extracelular.
Edema: exceso de líquido en los tejidos El edema se refiere a la presencia de un exceso de líquido en los tejidos corporales. En la mayoría de los casos el edema aparece sobre todo en el compartimiento de líquido extracelular, pero puede afectar también al líquido intracelular. Edema intracelular: Tres procesos causan especialmente tumefacción o edema intracelular:
1) la hiponatremia, según se ha comentado anteriormente; 2) la depresión de los sistemas metabólicos de los tejidos, y 3) la falta de una nutrición celular adecuada. Por ejemplo, cuando se reduce el flujo sanguíneo a un tejido, el reparto de oxígeno y nutrientes se reduce. Si el flujo sanguíneo disminuye mucho como para mantener el metabolismo normal tisular, se deprimen las bombas iónicas de la membrana celular. Cuando se activan las bombas, los iones sodio que normalmente se filtran hacia el interior de la célula ya no pueden salir bombeados de las células, y el exceso de sodio intracelular causas por ósmosis el paso del agua al interior de las células.
El edema intracelular también puede producirse en los tejidos inflamados. La inflamación suele aumentar la permeabilidad de las membranas celulares, lo que permite al sodio y a otros iones difundir hacia el interior de la célula, con la posterior entrada del agua por ósmosis al interior de las células. Edema extracelular El edema extracelular se produce cuando se acumula un exceso de líquido en los espacios extracelulares.
Hay dos causas generales de edema extracelular: 1) la fuga anormal de líquido del plasma hacia los espacios intersticiales a través de los capilares. 2) la imposibilidad de los linfáticos de devolver el líquido a la sangre desde el intersticio, lo que a menudo se conoce por linfedema. La causa clínica más común de la acumulación intersticial de líquido es la filtración capilar excesiva de líquido.
Linfedema:
Incapacidad de los vasos sanguíneos de devolver líquidos y proteínas a la sangre. Cuando la función de los vasos linfáticos está gravemente deteriorada, debido a una obstrucción o pérdida de dichos vasos, el edema puede ser especialmente intenso porque no hay otra forma de extraer las proteínas plasmáticas que salen al intersticio.
El aumento de la concentración de proteínas eleva la presión coloidosmótica del líquido intersticial, lo que arrastra incluso más líquido fuera de los capilares. El linfedema puede producirse también en personas que padecen ciertos tipos de cáncer o después de una intervención quirúrgica en que se eliminen u obstruyan vasos linfáticos. Por ejemplo, se elimina un gran número de ganglios linfáticos durante la mastectomía radical, lo que reduce la extracción de líquido de la mama y del brazo provocando un edema y tumefacción de los espacios tisulares. Unos pocos vasos linfáticos vuelven a crecer finalmente tras este tipo de intervención, de manera que el edema intersticial suele ser temporal.
Importancia del gel intersticial para evitar la acumulación de líquido en el intersticio
La importancia del gel es que impide que el líquido fluya fácilmente a través de los tejidos por el impedimento de «la superficie en cepillo» de billones de filamentos de proteoglucanos. Además, cuando la presión en el líquido intersticial se reduce a valores muy negativos, el gel no se contrae mucho porque la red de proteoglucanos ofrece una resistencia elástica a la compresión. Importancia de los filamentos de proteoglucanos como «espaciadores» para las células y para evitar el flujo rápido de líquido en los tejidos. Los filamentos de proteoglucano, junto con las fibrillas de colágeno mucho mayores que ocupan los espacios intersticiales, actúan como «espaciadores» entre las células.
Los nutrientes y los iones no difunden fácilmente a través de las membranas celulares; sin los espacios adecuados entre las células, estos nutrientes, electrólitos y productos de desecho celulares no podrían intercambiarse rápidamente entre los capilares sanguíneos y las células localizadas a distancia entre sí. Los filamentos de proteoglucanos también impiden que el líquido fluya con demasiada facilidad a través de los espacios tisulares. Si no fuera por los filamentos de proteoglucanos, el simple acto de levantarse causaría en una persona que grandes cantidades de líquido intersticial fluyeran desde la parte superior del cuerpo hacia la parte inferior.
Brandon nazario vazquez balanzar 1-B
FILTRACIÓN GLOMERULAR, FLUJO SANGUÍNEO RENAL Y SU CONTROL
FILTRACIÓN GLOMERULAR: EL PRIMER PASO PARA LA FORMACIÓN DE ORINA
El primer paso en la formación de orina es la filtración de grandes cantidades de líquidos a través de los capilares glomerulares en la cápsula de Bowman, casi 180 l al día. La mayor parte de este filtrado se reabsorbe, lo que deja únicamente 1 l aproximadamente de líquido para su excreción al día, si bien la tasa de excreción renal de líquidos puede ser muy variable dependiendo de la ingestión de líquidos. La alta tasa de filtración glomerular depende de la alta tasa de flujo sanguíneo renal, así como de las propiedades especiales de las membranas de los capilares glomerulares. En este capítulo se habla de las fuerzas físicas que determinan la filtración glomerular (FG), así como de los mecanismos fisiológicos que regulan la FG y el flujo sanguíneo renal.
Composición del filtrado glomerular
Como la mayoría de los capilares, los capilares glomerulares son relativamente impermeables a las proteínas, de manera que el líquido filtrado (llamado filtrado glomerular) carece prácticamente de proteínas y elementos celulares, incluidos los eritrocitos. Las concentraciones de otros constituyentes del filtrado glomerular, como la mayoría de las sales y moléculas orgánicas, son similares a las concentraciones en el plasma.
Las excepciones a esta generalización son algunas sustancias con un peso molecular bajo, como el calcio y los ácidos grasos, que no se filtran libremente porque están unidas parcialmente a las proteínas plasmáticas. Por ejemplo, casi la mitad del calcio plasmático y la mayor parte de los ácidos grasos plasmáticos están unidos a proteínas y estas porciones unidas no se filtran a través de los capilares glomerulares.
La FG es alrededor del 20% del flujo plasmático renal
La FG está determinada por:
1) El equilibrio entre las fuerzas hidrostáticas y coloidosmóticas que actúa a través de la membrana capilar.
2) El coeficiente de filtración capilar (Kf), el producto de la permeabilidad por el área superficial de filtro de los capilares.
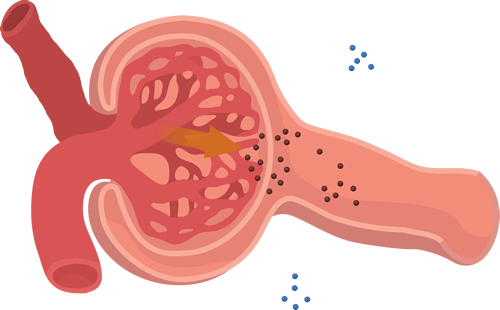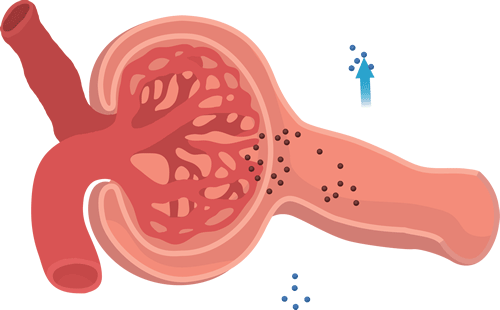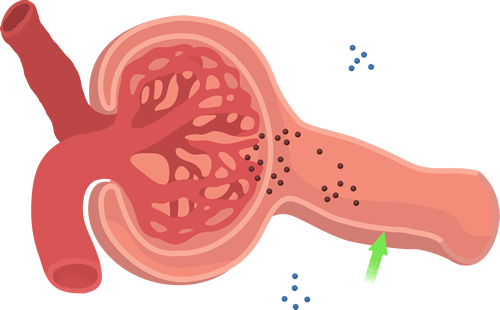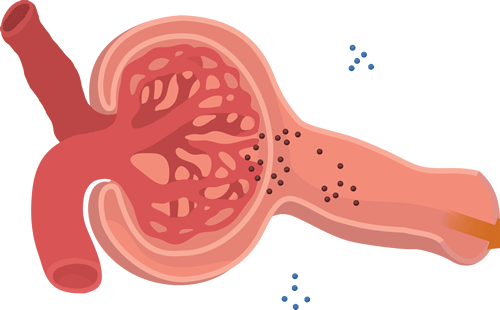
Los capilares glomerulares tienen una filtración mucho mayor que la mayoría de los otros capilares por una presión hidrostática glomerular alta y un gran Kf. En el adulto medio, la FG es de unos 125 ml/min, o 180 l/día. La fracción del flujo plasmático renal que se filtra (la fracción de filtración) es de media de 0,2, lo que significa que alrededor del 20% del plasma que fluye a través del riñón se filtra a través de los capilares glomerulares. La fracción de filtración se calcula como sigue:
MEMBRANA CAPILAR GLOMERULAR
La membrana capilar glomerular es similar a la de otros capilares, excepto en que tiene tres capas principales (en lugar de las dos habituales):
1) El endotelio del capilar.
2) Una membrana basal.
3) Una capa de células epiteliales (podocitos) rodeando a la superficie externa de la membrana basal capilar.
Juntas, estas capas forman la barrera de filtración que, a pesar de sus tres capas, filtra varios cientos de veces más agua y solutos que la membrana capilar habitual. Incluso con esta elevada intensidad de filtración, la membrana capilar glomerular evita normalmente la filtración de proteínas plasmáticas.
La elevada filtración a través de la membrana capilar glomerular se debe en parte a sus especiales características. El endotelio capilar está perforado por cientos de pequeños agujeros, llamados fenestraciones, similares a los capilares fenestrados que se encuentran en el hígado, aunque menores que las fenestraciones del hígado. Aunque la fenestración es relativamente grande, las proteínas celulares endoteliales están dotadas de muchas cargas negativas fijas que dificultan el paso de las proteínas plasmáticas.
Rodeando al endotelio está la membrana basal, que consta de una red de colágeno y fibrillas de proteoglucanos que tienen grandes espacios a través de los cuales pueden filtrarse grandes cantidades de agua y de solutos. La membrana basal evita con eficacia la filtración de proteínas plasmáticas, en parte debido a las cargas eléctricas negativas fuertes de los proteoglucanos.
La parte final de la membrana glomerular es una capa de células epiteliales que recubre la superficie externa del glomérulo. Estas células no son continuas, sino que tienen unas prolongaciones largas similares a pies (podocitos) que rodean la superficie externa de los capilares. Los podocitos están separados por espacios llamados poros en hendidura a través de los cuales se mueve el filtrado glomerular. Las células epiteliales, que tienen también cargas negativas, restringen de forma adicional la filtración de las proteínas plasmáticas. De este modo, todas las capas de la pared capilar glomerular proporcionan una barrera a la filtración de las proteínas plasmáticas.
La capacidad de filtración de los solutos se relaciona inversamente con su tamaño
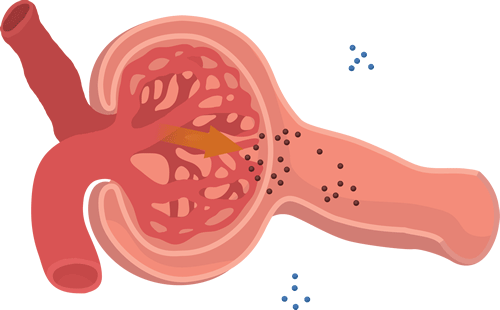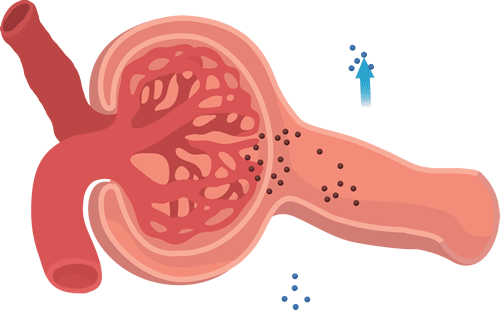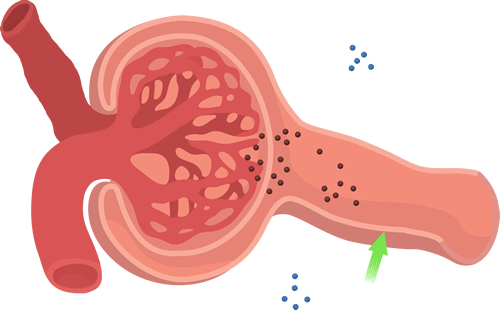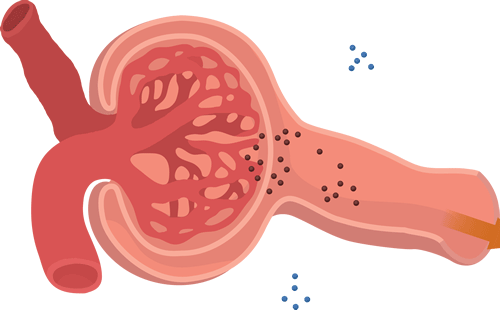
La membrana capilar glomerular es más gruesa que la de la mayoría de los otros capilares, pero es también mucho más porosa y por tanto filtra líquido con mayor intensidad. A pesar de la elevada filtración, la barrera de filtración glomerular filtra de modo selectivo las moléculas basándose en su tamaño y en su carga eléctrica.
Una capacidad de filtración de 1 significa que la sustancia se filtra tan libremente como el agua; una capacidad de filtración de 0,75 significa que la sustancia se filtra con una rapidez de solo un 75% la del agua. Obsérvese que los electrólitos como el sodio y los compuestos orgánicos pequeños como la glucosa se filtran libremente. A medida que la masa molecular de la molécula se acerca a la de la albúmina, su capacidad de filtración se reduce rápidamente, acercándose a cero.
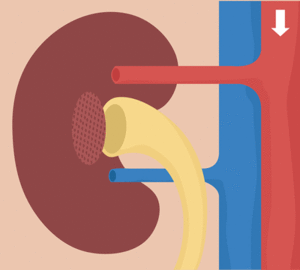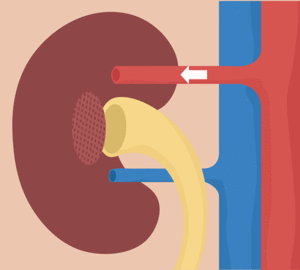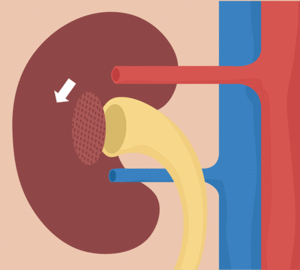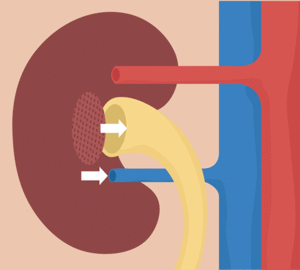
Las moléculas grandes con carga negativa se filtran con menor facilidad que las moléculas con el mismo tamaño molecular y cargas positivas
El diámetro molecular de la proteína plasmática albúmina es solo de unos 6 nm, mientras que los poros de la membrana glomerular tienen unos 8 nm (80 angstroms). Sin embargo, la albúmina no se filtra por su carga negativa y la repulsión electrostática ejercida por las cargas negativas de los proteoglucanos de la pared capilar glomerular.
La carga eléctrica afecta a la filtración en el glomérulo de dextranos con diferentes pesos moleculares. Los dextranos son polisacáridos que pueden fabricarse como moléculas neutras o con cargas positivas o negativas. Obsérvese que, para cualquier radio molecular, las moléculas con cargas positivas se filtran con mucha mayor facilidad que las moléculas con cargas negativas. Los dextranos neutros también se filtran con mayor facilidad que los dextranos con cargas negativas del mismo peso molecular.
En ciertas nefropatías, las cargas negativas que hay sobre la membrana basal se pierden incluso antes de que haya cambios notables en el aspecto histológico del riñón, un trastorno que se denomina nefropatía por cambios mínimos. La causa de esta pérdida de cargas negativas sigue sin estar clara, aunque se cree que está relacionada con una respuesta inmunitaria con secreción anómala por los linfocitos T de citocinas que reducen los aniones en las proteínas de los podocitos o en los capilares glomerulares. Como resultado de esta pérdida de cargas negativas en la membrana basal, algunas de las proteínas de peso molecular bajo, en especial la albúmina, se filtran y aparecen en la orina, un trastorno conocido como proteinuria o albuminuria. La nefropatía por cambios mínimos es más común en niños pequeños pero también puede aparecer en adultos, sobre todo en los afectados por trastornos autoinmunitarios.
DETERMINANTES DE LA FG
La FG está determinada por:
1) La suma de las fuerzas hidrostática y coloidosmótica a través de la membrana glomerular, que da lugar a la presión de filtración neta.
2) El coeficiente glomerular Kf.
En una fórmula matemática, la FG es igual al producto del Kf y de la presión de filtración neta:
La presión de filtración neta representa la suma de las fuerzas hidrostática y coloidosmótica que favorecen o se oponen a la filtración a través de los capilares glomerulares. Estas fuerzas son:
1) La presión hidrostática dentro de los capilares glomerulares (presión hidrostática glomerular, PG), que favorece la filtración.
2) La presión hidrostática en la cápsula de Bowman (PB) fuera de los capilares, que se opone a la filtración.
3) La presión coloidosmótica de las proteínas plasmáticas en el capilar glomerular (πG), que se opone a la filtración.
4) La presión coloidosmótica de las proteínas en la cápsula de Bowman (πB), que favorece la filtración. (En condiciones normales, la concentración de proteínas en el filtrado glomerular es tan baja que la presión coloidosmótica en el líquido de la cápsula de Bowman se considera cero.)
Aunque los valores normales para los determinantes de la FG no se han medido directamente en los seres humanos, se ha calculado en animales como los perros y las ratas. Basándonos en los resultados obtenidos en animales, se cree que las fuerzas normales aproximadas que favorecen y se oponen a la filtración glomerular en los seres humanos son como sigue:
Algunos de estos valores pueden cambiar mucho bajo diferentes condiciones fisiológicas, mientras que otras se alteran sobre todo en la enfermedad, como se expondrá más adelante
EL AUMENTO DEL COEFICIENTE DE FILTRACIÓN CAPILAR GLOMERULAR INCREMENTA LA FG
El Kf es una medida del producto de la conductividad hidráulica y el área superficial de los capilares glomerulares. El Kf no puede medirse directamente, pero se calcula experimentalmente dividiendo la FG entre la presión de filtración neta: Aunque el aumento del Kf eleva la FG y la reducción del Kf la reduce, los cambios en Kf probablemente no constituyen un mecanismo importante de regulación normal día a día de la FG. Pero algunas enfermedades reducen el Kf al reducir el número de capilares glomerulares funcionantes (reduciendo así el área superficial para la filtración) o aumentando el espesor de la membrana capilar glomerular y reduciendo su conductividad hidráulica.
Por ejemplo, la hipertensión incontrolada y la, diabetes mellitus reducen gradualmente el Kf al aumentar el espesor de la membrana basal capilar glomerular y, finalmente, dañando los capilares de forma tan grave que se pierde la función capilar.
El aumento de la presión hidrostática en la cápsula de Bowman reduce la FG
Las medidas directas, usando micropipetas, de la presión hidrostática en la cápsula de Bowman y en diferentes puntos del túbulo proximal en animales experimentales indican que una estimación razonable de la presión en la cápsula de Bowman en los seres humanos es de unos 18 mmHg en condiciones normales. El aumento de la presión hidrostática en la cápsula de Bowman reduce la FG, mientras que reducir la presión aumenta la FG. Pero los cambios en la presión de la cápsula de Bowman no son normalmente un mecanismo importante de regulación de la FG.
En ciertos estados patológicos asociados a la obstrucción de la vía urinaria, la presión en la cápsula de Bowman puede aumentar mucho y provocar una reducción grave de la FG. Por ejemplo, la precipitación del calcio o del ácido úrico puede dar lugar a «cálculos» que se alojen en la vía urinaria, a menudo en el uréter, lo que obstruye el flujo en la vía urinaria y aumenta la presión en la cápsula de Bowman. Esta situación reduce la FG y finalmente puede provocar hidronefrosis (distensión y dilatación de la pelvis y los cálices renales) y lesionar o incluso destruir el riñón a no ser que se alivie la obstrucción.
El aumento de la presión coloidosmótica capilar glomerular reduce la FG
A medida que la sangre pasa desde la arteriola aferente a través de los capilares glomerulares hasta las arteriolas eferentes, la concentración plasmática de las proteínas aumenta alrededor de un 20%. La razón de este aumento es que alrededor de una quinta parte del líquido en los capilares se filtra a la cápsula de Bowman, lo que concentra las proteínas plasmáticas glomerulares que no se filtran.
Suponiendo que la presión coloidosmótica normal del plasma que entra en los capilares glomerulares es de 28 mmHg, este valor habitualmente aumenta a unos 36 mmHg en el momento en que la sangre alcanza el extremo eferente de los capilares. Luego la presión coloidosmótica media de las proteínas plasmáticas en el capilar glomerular está a medio camino entre los 28 y los 36 mmHg, o unos 32 mmHg.
De este modo, dos factores que influyen en la presión coloidosmótica capilar glomerular son:
1) La presión coloidosmótica del plasma arterial.
2) La fracción de la plasma filtrada por los capilares glomerulares (fracción de filtración).
El aumento de la presión coloidosmótica del plasma arterial eleva la presión coloidosmótica capilar glomerular, lo que a su vez reduce la FG.
Aumentar la fracción de filtración también concentra las proteínas plasmáticas y eleva la presión coloidosmótica glomerular. Como la fracción de filtración se define como FG/flujo plasmático renal, la fracción de filtración puede aumentarse elevando la FG o reduciendo el flujo plasmático renal. Por ejemplo, una reducción del flujo plasmático renal sin cambio inicial en la FG tendería a aumentar la fracción de filtración, lo que aumentaría la presión coloidosmótica capilar glomerular y tendería a reducir la FG. Por esta razón, los cambios en el flujo sanguíneo renal pueden influir en la FG independientemente de los cambios en la presión hidrostática glomerular.
Al aumentar el flujo sanguíneo renal, una fracción menor del plasma se filtra inicialmente fuera de los capilares glomerulares, lo que provoca un incremento lento de la presión coloidosmótica glomerular y un menor efecto inhibidor sobre la FG. En consecuencia, incluso con una presión hidrostática glomerular constante, una mayor cantidad de flujo sanguíneo hacia el glomérulo tiende a aumentar la FG, y una menor intensidad del flujo sanguíneo hacia el glomérulo tiende a reducirla.
El aumento de la presión hidrostática capilar glomerular incrementa la FG
Se ha calculado que la presión hidrostática capilar glomerular es de unos 60 mmHg en condiciones normales. Los cambios en la presión hidrostática glomerular son la principal forma de regular fisiológicamente la FG. Los aumentos en la presión hidrostática glomerular incrementan la FG, mientras que las reducciones en la presión hidrostática glomerular la reducen.
La presión hidrostática glomerular está determinada por tres variables, todas ellas bajo control fisiológico:
1) Presión arterial.
2) Resistencia arteriolar aferente.
3) Resistencia arteriolar eferente.
El aumento de la presión arterial tiende a elevar la presión hidrostática glomerular y, por tanto, a aumentar la FG. (Sin embargo, como se comentará después, este efecto está amortiguado por mecanismos autorreguladores que mantienen una presión glomerular relativamente constante mientras fluctúa la presión arterial.)
El aumento de la resistencia en las arteriolas aferentes reduce la presión hidrostática glomerular y disminuye la FG. Por el contrario, la dilatación de las arteriolas aferentes aumenta la presión hidrostática glomerular y la FG. La constricción de las arteriolas eferentes aumenta la resistencia al flujo de salida de los capilares glomerulares.
Este mecanismo incrementa la presión hidrostática glomerular, y mientras que el aumento de la resistencia eferente no reduzca demasiado el flujo sanguíneo renal, la FG se eleva ligeramente. Sin embargo, como la constricción arteriolar aferente también reduce el flujo sanguíneo renal, la fracción de filtración y la presión coloidosmótica glomerular aumentan a medida que la resistencia arteriolar eferente aumenta. Por tanto, si la constricción de las arteriolas eferentes es intensa (incremento mayor de tres veces de la resistencia arteriolar eferente), el aumento de la presión coloidosmótica supera el incremento de la presión hidrostática capilar glomerular debido a la constricción arteriolar eferente. Cuando se produce esta situación, la fuerza neta de la filtración se reduce en realidad, lo que disminuye la FG.
De este modo, la constricción arteriolar eferente tiene un efecto bifásico sobre la FG. Con niveles moderados de constricción la FG se incrementa ligeramente, pero con una constricción intensa, se reduce. La principal causa de la reducción final de la FG es la que sigue. A medida que la constricción eferente aumenta y la concentración de las proteínas plasmáticas aumenta, se produce un incremento no lineal rápido en la presión coloidosmótica debido al efecto Donnan; cuanto mayor es la concentración de proteínas, más rápidamente aumenta la presión coloidosmótica debido a la interacción de los iones unidos a las proteínas plasmáticas, que también ejercen un efecto osmótico.
FLUJO SANGUÍNEO RENAL
En un hombre de 70 kg, el flujo sanguíneo combinado a través de los dos riñones es de unos 1.100 ml/min, o un 22% del gasto cardíaco. Considerando el hecho de que los dos riñones constituyen solo alrededor del 0,4% del peso total del cuerpo, podemos percibir fácilmente que reciben un flujo extremadamente grande de sangre comparados con otros órganos.
Como en otros tejidos, el flujo sanguíneo aporta a los riñones nutrientes y se lleva los productos de desecho. Pero el elevado flujo renal supera mucho sus necesidades. El objetivo de este flujo adicional es aportar suficiente plasma para la elevada filtración glomerular necesaria para una regulación precisa de los volúmenes del líquido corporal y las concentraciones de solutos. Como podría esperarse, los mecanismos que regulan el flujo sanguíneo renal están muy ligados al control de la FG y a las funciones excretoras de los riñones.
FLUJO SANGUÍNEO RENAL Y CONSUMO DE OXÍGENO
Con respecto al gramo de peso, los riñones consumen normalmente el doble de oxígeno que el encéfalo, pero tienen casi siete veces más flujo sanguíneo. Luego el oxígeno transportado a los riñones supera con mucho sus necesidades metabólicas, y la extracción arteriovenosa de oxígeno es relativamente baja comparada con la de la mayor parte de los restantes tejidos.
Una gran fracción del oxígeno consumido por los riñones se relaciona con la elevada reabsorción del sodio en los túbulos renales. Si el flujo renal y la FG se reducen y se filtra menos sodio, se reabsorbe menos sodio y se consume menos oxígeno. Por tanto, el consumo renal de oxígeno varía en proporción con la reabsorción tubular renal de sodio, que a su vez está muy relacionada con la FG y la velocidad de filtración del sodio. Si la filtración glomerular cesa por completo, también lo hace la reabsorción renal de sodio, y el consumo de oxígeno se reduce a una cuarta parte de lo normal. Este consumo residual de oxígeno refleja las necesidades metabólicas de las células renales.
DETERMINANTES DEL FLUJO SANGUÍNEO RENAL
El flujo sanguíneo renal está determinado por el gradiente de presión a través de los vasos renales (la diferencia entre las presiones hidrostáticas en la arteria renal y en la vena renal), dividido entre la resistencia vascular total renal: La presión en la arteria renal es aproximadamente igual a la presión arterial sistémica, y la presión en la vena renal es de media de 3-4 mmHg en la mayoría de las condiciones. Como en otros lechos vasculares, la resistencia vascular total a través de los riñones está determinada por la suma de las resistencias en segmentos vasculares individuales, incluidas las arterias, las arteriolas, los capilares y las venas. La mayor parte de la resistencia vascular renal reside en tres segmentos principales: las arterias interlobulillares, las arterias aferentes y las arteriolas eferentes.
La resistencia de estos vasos está controlada por el sistema nervioso simpático, varias hormonas y mecanismos de control locales internos, como se comentará más adelante. Un aumento de la resistencia en cualquiera de los segmentos vasculares de los riñones tiende a reducir el flujo sanguíneo renal, mientras que una reducción en la resistencia vascular aumenta el flujo sanguíneo renal si las presiones en la vena y arteria renales permanecen constantes. Aunque los cambios en la presión arterial ejercen cierta influencia sobre el flujo sanguíneo renal, los riñones tienen mecanismos efectores para mantener el flujo sanguíneo renal y la FG relativamente constantes entre los 80 y 170 mmHg de presión arterial, un proceso llamado autorregulación. Esta capacidad de autorregulación se produce a través de mecanismos que son completamente intrínsecos
EL FLUJO SANGUÍNEO EN LOS VASOS RECTOS DE LA MÉDULA RENAL ES MUY BAJO COMPARADO CON EL FLUJO EN LA CORTEZA RENAL
La parte externa del riñón, la corteza renal, recibe la mayor parte del flujo sanguíneo renal. El flujo sanguíneo en la médula renal supone solo el 1-2% del flujo sanguíneo renal total. El flujo en la médula renal procede de una porción especializada del sistema capilar peritubular llamada vasos rectos. Estos vasos descienden hasta la médula paralelos a las asas de Henle y después vuelven de nuevo junto a las asa de Henle hasta la corteza antes de vaciarse en el sistema venoso, los vasos rectos son importantes para que los riñones puedan formar una orina concentrada.
CONTROL FISIOLÓGICO DE LA FILTRACIÓN GLOMERULAR Y DEL FLUJO SANGUÍNEO RENAL
Los determinantes de la FG que son más variables y están sujetos al control fisiológico son la presión hidrostática glomerular y la presión coloidosmótica capilar glomerular. Estas variables, a su vez, están influenciadas por el sistema nervioso simpático, las hormonas y los autacoides (sustancias vasoactivas que liberan los riñones y actúan a nivel local) y otros controles de retroalimentación que son intrínsecos a los riñones.
LA INTENSA ACTIVACIÓN DEL SISTEMA NERVIOSO SIMPÁTICO REDUCE LA FG
Casi todos los vasos sanguíneos de los riñones, incluidas las arteriolas aferentes y eferentes, están muy inervados por fibras nerviosas simpáticas. La fuerte activación de los nervios simpáticos renales puede contraer las arteriolas renales y reducir el flujo sanguíneo renal y la FG. La estimulación moderada o leve ejerce poca influencia sobre el flujo sanguíneo renal y la FG.
Por ejemplo, la activación refleja del sistema nervioso simpático debida a descensos moderados de la presión en los barorreceptores del seno carotídeo o en los receptores cardiopulmonares ejerce poca influencia sobre el flujo sanguíneo renal o la FG. Sin embargo, incluso aumentos ligeros en la actividad simpática renal pueden provocar un descenso en la excreción de sodio y agua al incrementar la reabsorción tubular renal. Los nervios simpáticos renales parecen más importantes para reducir la FG durante los trastornos agudos y graves que duran de varios minutos a unas pocas horas, como los provocados por las reacciones de defensa, la isquemia encefálica o la hemorragia grave. En la persona sana en reposo, el tono simpático ejerce poca influencia sobre el flujo sanguíneo renal.
CONTROL HORMONAL Y POR AUTACOIDES DE LA CIRCULACIÓN RENAL
La noradrenalina, la adrenalina y la endotelina contraen los vasos sanguíneos renales y reducen la FG
Las hormonas que constriñen las arteriolas aferentes y eferentes, lo que reduce la FG y el flujo sanguíneo renal, son la noradrenalina y la adrenalina liberadas por la médula suprarrenal. Las concentraciones sanguíneas de estas hormonas van generalmente paralelas a la actividad del sistema nervioso simpático; luego la noradrenalina y la adrenalina ejercen escasa influencia sobre la hemodinámica renal excepto en condiciones extremas, como una hemorragia grave.
Otro vasoconstrictor, la endotelina, es un péptido que pueden liberar las células endoteliales vasculares lesionadas de los riñones, así como de otros tejidos. La función fisiológica de estos autacoides no se conoce del todo. Pero la endotelina puede contribuir a la hemostasia (minimizando la pérdida de sangre) cuando se secciona un vaso sanguíneo, lo que lesiona el endotelio y libera este poderoso vasoconstrictor. Las concentraciones plasmáticas de endotelina también aumentan en muchas enfermedades asociadas a lesiones vasculares, como la toxemia del embarazo, la insuficiencia renal aguda y la uremia crónica, y pueden contribuir a la vasoconstricción renal y reducir la FG en algunas de estas alteraciones fisiopatológicas.
La angiotensina II contrae preferentemente las arteriolas eferentes en la mayoría de los estados fisiológicos
Un vasoconstrictor renal poderoso, la angiotensina II, puede considerarse una hormona circulante y un autacoide local porque se forma en los riñones y en la circulación sistémica. Los receptores para angiotensina II están presentes prácticamente en todos los vasos sanguíneos. No obstante, los vasos sanguíneos preglomerulares, en especial las arteriolas aferentes, parecen estar relativamente protegidos de la contracción mediada por angiotensina II en la mayoría de los estados fisiológicos asociados con la activación del sistema renina-angiotensina (p. ej., durante una dieta baja en sodio o una presión de perfusión renal reducida debida a estenosis de la arteria renal). Esta protección se debe a la liberación de vasodilatadores, especialmente óxido nítrico y prostaglandinas, que contrarrestan los efectos vasoconstrictores de angiotensina II en esos vasos sanguíneos.
Sin embargo, las arteriolas eferentes son altamente sensibles a la angiotensina II. Debido a que la angiotensina II contrae sobre todo las arteriolas eferentes en la mayoría de los estados fisiológicos, las concentraciones de angiotensina II aumentadas elevan la presión hidrostática glomerular mientras reducen el flujo sanguíneo renal. Debe tenerse en cuenta que la mayor formación de angiotensina II suele tener lugar en situaciones que se acompañan de una reducción de la presión arterial o una pérdida de volumen, que tienden a reducir la FG. En estas circunstancias, la mayor concentración de angiotensina II, al constreñir las arteriolas eferentes, ayuda a evitar reducciones de la presión hidrostática glomerular y de la FG; al mismo tiempo, la reducción del flujo sanguíneo renal causada por la constricción arteriolar eferente contribuye a reducir el flujo a través de los capilares peritubulares, lo que a su vez aumenta la reabsorción de sodio y de agua.
De este modo, el aumento de la concentración de angiotensina II que aparece en las dietas pobres en sodio o en las pérdidas de volumen ayuda a mantener la FG y la excreción normal de productos de desecho metabólicos, como la urea y la creatinina, que dependen de la filtración glomerular para su secreción; al mismo tiempo, la constricción inducida por la angiotensina II de las arteriolas eferentes incrementa la reabsorción tubular de sodio y agua, lo que ayuda a restaurar el volumen sanguíneo y la presión arterial. Este efecto de la angiotensina II para ayudar a «autorregular» la FG.
El óxido nítrico derivado del endotelio reduce la resistencia vascular renal y aumenta la FG
Un autacoide que reduce la resistencia vascular renal y es liberado por el endotelio vascular de todo el cuerpo es el óxido nítrico derivado del endotelio. La producción basal de óxido nítrico parece importante para mantener la vasodilatación de los riñones, ya que permite a los riñones excretar cantidades normales de sodio y de agua. La administración de fármacos que inhiban esta formación normal de óxido nítrico incrementará la resistencia vascular renal y reducirá la FG y la excreción urinaria de sodio, lo que finalmente elevará la presión arterial. En algunos pacientes hipertensos o en pacientes con ateroesclerosis, los daños en el endotelio vascular y el deterioro en la producción de óxido nítrico podrían ser la causa de la vasoconstricción renal y de la elevación de la presión arterial.
Las prostaglandinas y la bradicinina reducen la resistencia vascular renal y tienden a aumentar la FG
Las hormonas y los autacoides que producen vasodilatación y aumentan el flujo sanguíneo renal y la FG son las prostaglandinas (PGE2 y PGI2) y la bradicinina.
Aunque estos vasodilatadores no parecen tener mucha importancia en la regulación del flujo sanguíneo renal ni de la FG en condiciones normales, pueden amortiguar los efectos vasoconstrictores de los nervios simpáticos o de la angiotensina II, en especial sus efectos constrictores sobre las arteriolas aferentes.
Al oponerse a la vasoconstricción de las arteriolas aferentes, las prostaglandinas pueden ayudar a evitar reducciones excesivas de la FG y del flujo sanguíneo renal. En condiciones de estrés, como la pérdida de volumen o tras una intervención quirúrgica, la administración de antiinflamatorios no esteroideos, como ácido acetilsalicílico, que inhiben la síntesis de prostaglandinas puede reducir significativamente la FG.
AUTORREGULACIÓN DE LA FG Y DEL FLUJO SANGUÍNEO RENAL
Los mecanismos de retroalimentación intrínsecos de los riñones mantienen normalmente el flujo sanguíneo renal y la FG relativamente constantes, a pesar de cambios acentuados en la presión arterial sistémica. Estos mecanismos todavía funcionan en los riñones perfundidos con sangre que se han extraído del cuerpo, independientes de las influencias sistémicas. Esta constancia relativa de la FG y del flujo sanguíneo renal se denomina autorregulación.
La principal función de la autorregulación del flujo sanguíneo en la mayoría de los tejidos diferentes a los riñones es mantener el reparto de oxígeno y nutrientes en valores normales y la extracción de los productos de desecho del metabolismo, a pesar de los cambios en la presión arterial. En los riñones, el flujo sanguíneo normal es mucho mayor que el necesario para estas funciones. La principal función de la autorregulación en los riñones es mantener una FG relativamente constante que permita un control preciso de la excreción renal de agua y de solutos.
La FG permanece normalmente autorregulada (es decir, relativamente constante) a pesar de las fluctuaciones considerables de la presión arterial que se producen durante las actividades usuales de una persona. Por ejemplo, una reducción en la presión arterial hasta tan solo 70 a 75 mmHg o un incremento de hasta 160 a 180 mmHg cambia habitualmente la FG menos del 10%. En general, el flujo sanguíneo renal se autorregula en paralelo con la FG, pero la FG se autorregula de forma más eficiente en ciertas condiciones.
IMPORTANCIA DE LA AUTORREGULACIÓN DE LA FG PARA EVITAR CAMBIOS EXTREMOS EN LA EXCRECIÓN RENAL.
Aunque los mecanismos autorreguladores renales no son perfectos, impiden cambios potencialmente grandes de la FG y de la excreción renal de agua y solutos que de otro modo se producirían con los cambios de la presión arterial. Podemos entender la importancia cuantitativa de la autorregulación al considerar las magnitudes relativas de la filtración glomerular, la reabsorción tubular y la excreción renal, y los cambios en la excreción renal que podrían tener lugar sin los mecanismos autorreguladores.
La FG es normalmente de 180 l/día y la reabsorción tubular de 178,5 l/día, lo que deja 1,5 l/día de líquido que se excreta en la orina. Si no hubiera ninguna autorregulación, un incremento relativamente pequeño en la presión arterial (de 100 a 125 mmHg) provocaría un incremento similar de un 25% en la FG (de unos 180 a 225 l/día). Si la reabsorción tubular permaneciera constante en 178,5 l/día, el flujo de orina aumentaría a 46,5 l/día (la diferencia entre la FG y la reabsorción tubular), un incremento total de la orina de más de 30 veces. Debido a que el volumen total de plasma es solo de unos 3 l, tal cambio agotaría rápidamente el volumen sanguíneo.
En realidad, los cambios en la presión arterial suelen ejercer un efecto mucho menor sobre el volumen de orina por dos razones:
1) La autorregulación renal impide los grandes cambios en la FG que de otra forma se producirían.
2) Hay mecanismos adaptativos adicionales en los túbulos renales que provocan un incremento de su reabsorción cuando la FG aumenta, un fenómeno llamado equilibrio glomerulotubular.
Incluso con estos mecanismos de control especiales, los cambios en la presión arterial todavía ejercen efectos significativos sobre la excreción renal de agua y de sodio; a esto se le denomina diuresis por presión o natriuresis por presión, y es crucial en la regulación de los volúmenes del líquido corporal y de la presión arterial.
RETROALIMENTACIÓN TUBULOGLOMERULAR Y AUTORREGULACIÓN DE LA FG
Los riñones tienen un mecanismo especial de retroalimentación que acopla los cambios en la concentración de cloruro de sodio en la mácula densa al control de la resistencia arteriolar renal y la autorregulación de la FG. Esta retroalimentación ayuda a asegurar una llegada relativamente constante de cloruro de sodio al túbulo distal y ayuda a evitar las fluctuaciones falsas en la excreción renal que de otro modo tendrían lugar. En muchas circunstancias, esta retroalimentación autorregula el flujo sanguíneo renal y la FG en paralelo. Pero debido a que este mecanismo se dirige específicamente a estabilizar la llegada de cloruro de sodio al túbulo distal, hay casos en que la FG se autorregula a expensas de cambiar el flujo sanguíneo renal, como se comenta más adelante. En otros casos, este mecanismo puede inducir realmente cambios en la FG como respuesta a cambios primarios en la reabsorción de cloruro de sodio en los túbulos renales.
El mecanismo de retroalimentación tubuloglomerular tiene dos componentes que actúan juntos en el control de la FG:
1) Un mecanismo de retroalimentación arteriolar aferente.
2) Un mecanismo de retroalimentación arteriolar eferente.
Estos mecanismos de retroalimentación dependen de disposiciones anatómicas especiales del complejo yuxtaglomerular.
El complejo yuxtaglomerular consta de las células de la mácula densa en la porción inicial del túbulo distal y las células yuxtaglomerulares en las paredes de las arteriolas aferentes y eferentes. La mácula densa es un grupo especializado de células epiteliales en los túbulos distales que entra en estrecho contacto con las arteriolas aferente y eferente. Las células de la mácula densa contienen aparato de Golgi, que son orgánulos secretores intracelulares dirigidos hacia las arteriolas, lo que indica que estas células pueden estar secretando una sustancia hacia ellas.
La reducción del cloruro de sodio en la mácula densa dilata las arteriolas aferentes y aumenta la liberación de renina
Las células de la mácula densa perciben cambios en el volumen que llega al túbulo distal por medio de señales que no se conocen del todo. Los estudios experimentales hacen pensar que la reducción de la FG disminuye la velocidad del flujo que llega al asa de Henle, lo que aumenta la reabsorción del porcentaje de iones sodio y cloro suministrados a la rama ascendente del asa de Henle, hecho que disminuye la concentración de cloruro de sodio en las células de la mácula densa. Esta reducción de la concentración de cloruro de sodio inicia una señal que parte de la mácula densa y tiene dos efectos:
1) Reduce la resistencia al flujo sanguíneo en las arteriolas aferentes, lo que eleva la presión hidrostática glomerular y ayuda a normalizar la FG.
2) Aumenta la liberación de renina en las células yuxtaglomerulares de las arteriolas aferente y eferente, que son los principales reservorios de renina.
La renina liberada de estas células actúa después como una enzima aumentando la formación de angiotensina I, que se convierte en angiotensina II. Finalmente, la angiotensina II contrae las arteriolas eferentes, con lo que aumenta la presión hidrostática glomerular y ayuda a normalizar la FG.
Estos dos componentes del mecanismo de retroalimentación tubuloglomerular, que operan juntos por medio de la estructura anatómica especial del aparato yuxtaglomerular, proporcionan señales de retroalimentación a las arteriolas aferente y eferente para una autorregulación eficiente de la FG durante los cambios de la presión arterial. Cuando ambos mecanismos funcionan juntos, la FG cambia solo unos puntos porcentuales, incluso con grandes fluctuaciones de la presión arterial entre los límites de 75 y 160 mmHg.
AUTORREGULACIÓN MIÓGENA DEL FLUJO SANGUÍNEO RENAL Y DE LA FG
Otro mecanismo que contribuye al mantenimiento del flujo sanguíneo renal y de la FG relativamente constantes es la capacidad de cada vaso sanguíneo de resistirse al estiramiento durante el aumento de la presión arterial, un fenómeno denominado mecanismo miógeno. Los estudios realizados en vasos individuales (sobre todo en arteriolas pequeñas) de todo el cuerpo han demostrado que responden a un aumento de la tensión o un estiramiento de la pared con una contracción del músculo liso vascular. El estiramiento de la pared vascular permite un mayor movimiento de los iones calcio desde el líquido extracelular hacia las células, lo que provoca su contracción por medio de unos mecanismos. Esta contracción impide una distensión excesiva de la pared y al mismo tiempo, mediante un aumento de la resistencia vascular, ayuda a impedir un aumento excesivo del flujo sanguíneo renal y de la FG cuando la presión arterial aumenta.
Aunque el mecanismo miógeno opera probablemente en la mayoría de las arteriolas del cuerpo, su importancia en la autorregulación del flujo sanguíneo renal y de la FG ha sido cuestionada por algunos fisiólogos porque este mecanismo sensible a la presión no tiene medio de detectar directamente por sí mismo cambios en el flujo sanguíneo renal ni en la FG. Por otra parte, este mecanismo puede ser más importante para proteger el riñón de lesiones inducidas por hipertensión. Como respuesta a aumentos repentinos en la presión sanguínea, la respuesta de contracción miógena en las arteriolas aferentes tiene lugar en unos segundos y, por tanto, atenúa la transmisión del aumento de la presión arterial a los capilares glomerulares.
Brandon vazquez balanzar 1-B
FUNCION DOMINANTE DE LOS RIÑONES EN EL CONTROL A LARGO PLAZO DE LA PRESION ARTERIAL Y EN LA HIPERTENSION: EL SISTEMA INTEGRADO DE REGULACION DE LA PRESION ARTERIAL.
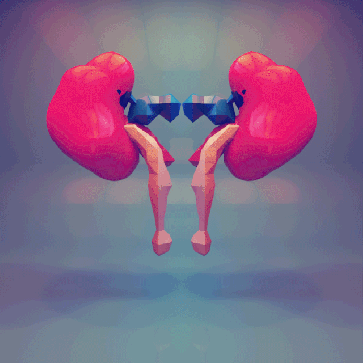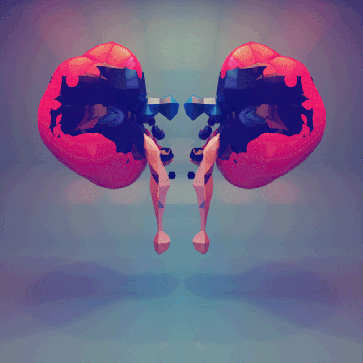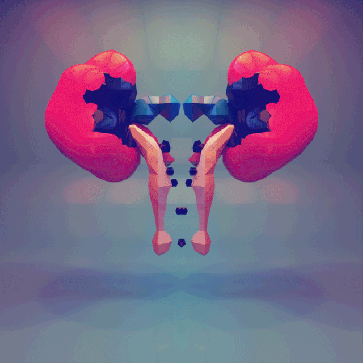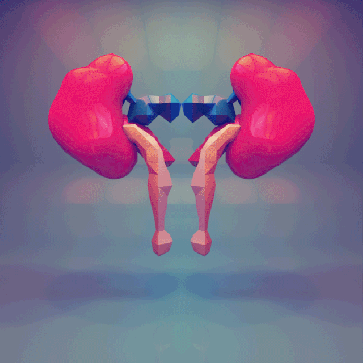
El sistema nervioso simpático desempeña un papel muy importante en la regulación a corto plazo de la presión arterial principalmente a través de los efectos del sistema nervioso sobre la resistencia vascular periférica total y la capacitancia y sobre la capacidad de la bomba cardiaca. Sin embargo, el organismo también dispone de mecanismos potentes para regular la presión arterial semana tras semana y mes tras mes. Este control a largo plazo de la presión arterial esta íntimamente relacionado con la homeostasis del volumen de liquido en el organismo, que esta determinada por el balance entre la ingestión y eliminación de líquidos.
SISTEMA DE LÍQUIDOS RENAL-CORPORAL PARA EL CONTROL DE LA PRESIÓN ARTERIAL
El sistema de líquidos renal-corporal para el control de la presión arterial actua de forma lenta, pero muy poderosa, del modo siguiente: si el volumen de sangre aumenta y la capacitancia vascular no se ve alterada, la presión arterial también aumenta. A su vez, el aumento de la presión hace que los riñones excreten el exceso de volumen, con lo que la presión se normaliza.
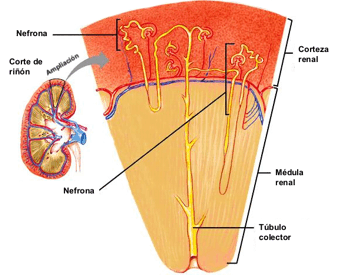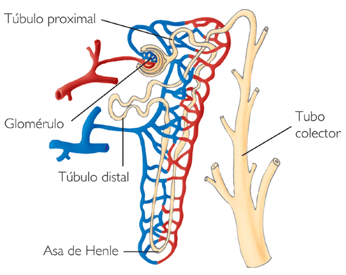
CUANTIFICACIÓN DE LA DIURESIS POR PRESIÓN COMO BASE DEL CONTROL DE LA PRESIÓN ARTERIAL.
Se muestra el efecto medio aproximado de distintos niveles de presión arterial sobre la eliminación de volumen por orina en el riñón aislado, demostrándose un aumento importante de volumen de orina es el fenómeno de diuresis por presión. La curva de esta figura se conoce como curva de eliminación de orina en el riñón, o curva de función renal.
El el ser humano la eliminación de orina con una presión arterial de 50 mmHg es esencialmente cero. Con 100 mmHg es normal y con 200 mmHg es entre seis y ocho veces mas de lo normal. Además, no solo el aumento de la presión arterial aumenta la producción de volumen de orina, sino que también provoca un aumento aproximadamente igual de la eliminación de sodio, que es el fenómeno de natriuresis por presión.
EL MECANISMO DE CONTROL DE LÍQUIDOS RENAL-CORPORAL PROPORCIONA UNA GANANCIA POR RETROALIMENTACIÓN CASI INFINITA PARA EL CONTROL DE LA PRESIÓN ARTERIAL A LARGO PLAZO.
Se muestra un método grafico que se puede usar para analizar el control de la presión arterial por el sistema de liquidos renal-corporal. Este análisis se basa en dos curvas independientes que se cruzan: 1) la curva de eliminación renal de agua y sal en respuesta al aumento de la presión arterial, que es la misma curva de eliminación renal, 2) la curva (o línea) que representa la ingestión neta de agua y sal.
DOS DETERMINANTES CLAVE DE LA PRESION ARTERIAL A LARGO PLAZO.
Mientras que las dos curvas que representan: 1) la eliminación renal de sal y agua, y 2) la ingestión de sal y agua, la presión arterial media a largo plazo al final se reajustará exactamente hasta 100 mmHg, que es el nivel de presión representado por el punto de equilibrio. Hay solo dos formas en las que la presión de este punto de equilibrio puede cambiar a partir de los 100 mmHg. Uno de ellos es el desplazamiento del nivel de presión de la curva de eliminación renal de sal y agua y el otro es el cambio de la línea de ingestión de agua y sal.
LA CURVA DE ELIMINACIÓN RENAL CRÓNICA ES MUCHO MÁS PRONUNCIADA QUE LA CURVA AGUDA.
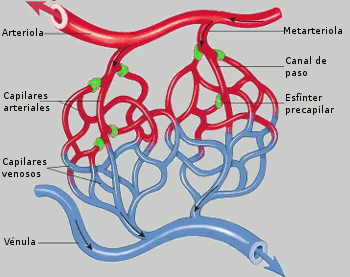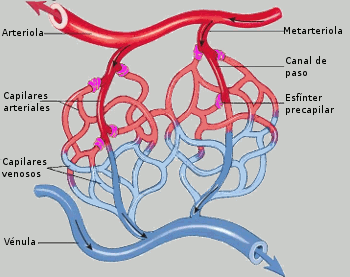
Una característica importante de la natriuresis por presión (y la diuresis por presión) es que los cambios crónicos en la presión arterial, que duran días o meses, tienen un efecto muy superior sobre la eliminación renal de sal y agua que el observado durante los cambios agudos de presión. Es decir, cuando los riñones funcionan normalmente, la curva de eliminación renal crónica es mucho mas pronunciada que la curva aguda.
Los poderosos efectos de los aumentos crónicos en la presión renal sobre la eliminación de orina se deben a que el aumento de la presión no solo tiene efectos hemodinámicos directos en los riñones para incrementar la excreción, sino también efectos indirectos mediados por cambios nerviosos y hormonales que tienen lugar cuando aumenta la presión de la sangre.
La importancia de las influencias neurales y hormonales en la natriuresis por presión es evidente especialmente durante los cambios crónicos en la ingestión de sodio. Si los riñones y los mecanismos nerviosos y hormonales están funcionando con normalidad, los aumentos crónicos en la ingestión de sal y agua de hasta seis veces los valores normales se asocian comúnmente con incrementos pequeños en la presión arterial.
FRACASO DEL AUMENTO DE LA RESISTENCIA PERIFERICA TOTAL PARA ELEVAR A LARGO PLAZO LA PRESION ARTERIAL SI NO SE MODIFICAN LA INGESTION DE LÍQUIDOS Y LA FUNCIÓN RENAL.
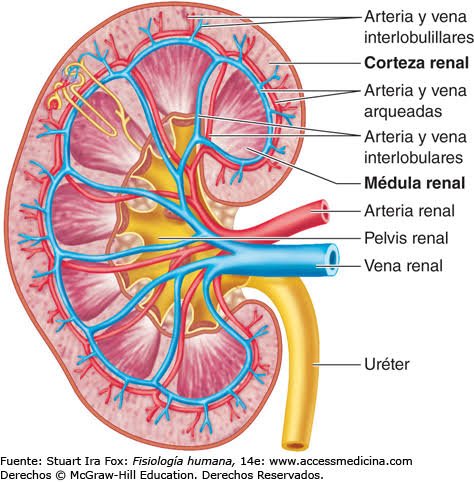
Recordando la ecuación básica de que la presión arterial (la presión arterial es igual al gasto cardiaco por la resistencia periférica total), esta claro que el aumento de la resistencia periférica total debería elevar la presión arterial. En realidad, la presión arterial aumenta inmediatamente cuando la resistencia periférica total aumenta de forma aguda. En este momento, la elevación aguda de la presión arterial no se mantiene si los riñones continúan funcionando normalmente, por el contrario retorna a la normalidad en 1 dia, mas o menos.
La razón de que se produzca este fenómeno es el aumento de la resistencia vascular de los vasos sanguíneos en todo el organismo además de en los riñones no cambia el punto de equilibrio para el control de la presión arterial que dictan los riñones. Por el contrario, los riñones comienzan inmediatamente a responder a la presión arterial alta, provocando la diuresis por presión y la natriuresis por presión.
EL AUMENTO DE VOLUMEN DE LÍQUIDO PUEDE ELEVAR LA PRESIÓN ARTERIAL AL AUMENTAR EL GASTO CARDIACO O LA RESISTENCIA PERIFÉRICA TOTAL.
El mecanismo global por el que el volumen aumentado del líquido extracelular puede elevar la presión arterial, si la capacidad vascular no se incrementa simultáneamente. La secuencia es la siguiente: 1) el aumento de volumen del líquido extracelular 2) aumenta el volumen de sangre, que a su vez 3) aumenta la presión de llenado media de la circulación, que a su vez 4) aumenta el retorno venoso de sangre hacia el corazón, que a su vez 5) aumenta el gasto cardiaco, que a su vez 6) aumenta la presión arterial. A su vez, el aumento en la presión arterial incrementa la excreción renal de sal y agua y puede devolver el volumen de líquido extracelular a valores casi normales si la función renal es normal.
IMPORTANCIA DE LA SAL (NaCl) EN EL ESQUEMA RENAL-LÍQUIDO CORPORAL DE REGULACIÓN DE LA PRESIÓN ARTERIAL.
El motivo de este hallazgo es que el agua pura se excreta normalmente por los riñones casi con la misma velocidad con la que se ingiere, mientras que la sal no se excreta tan fácilmente. A medida que se acumula la sal en el organismo aumenta indirectamente el volumen de líquido extracelular, por dos razones básicas:
1) Cuando hay un exceso de sal en el liquido extracelular aumenta la osmolalidad de líquido, lo que, a su vez, estimula el centro de sed en el cerebro, haciendo que esta persona beba cantidades extra de agua para normalizar la concentración extracelular de sal, aumentando el volumen de liquido extracelular.
2) El aumento de la osmolalidad causado por el exceso de sal en el liquido extracelular también estimula el mecanismo secretor del eje hipotálamo-hipófisis porterior para segregar cantidades mayores de hormona antidiurética.
LA HIPERTENSIÓN CRÓNICA SE DEBE A UN DETERIORO DE LA FUNCIÓN RENAL.
Cuando se dice que una persona tiene hipertensión crónica (o <>) ¡, quiere decirse que su presión arterial media es mayor que el limite superior del intervalo de las mediciones que se aceptan como normales. Una presión arterial media mayor de 110 mmHg (la normal es de 90 mmHg) se considera hipertensión. (Este nivel de presión arterial media aparece cuando la presión arterial diastólica es mayor de 90 mmHg y la presión sistólica es mayor de 135 mmHg). En personas con hipertensión importante, la presión arterial media aumenta hasta 150-170 mmHg, con una presión diastólica hasta de 130 mmHg y una presión sistólica que, en ocasiones, puede llegar a los 250 mmHg.
HIPERTENSIÓN POR SOBRECARGA DE VOLUMEN EN PACIENTES QUE NO TIENEN RIÑONES, PERO QUE SE MANTIENEN CON UN RIÑÓN ARTIFICIAL.
En los pacientes que se mantienen con un riñon artificial es especialmente importante mantener el volumen de liquido corporal en un nivel normal mediante la retirada de una cantidad apropiada de agua y sal cada vez que el paciente se somete a diálisis. Si no se actúa de este modo y se deja aumentar el volumen de liquido extracelular, casi invariablemente se producirá hipertensión.
HIPERTENSIÓN PROVOCADA POR EL EXCESO DE ALDOSTERONA.
Otro tipo de hipertensión por sobrecarga de volumen se debe a un exceso de aldosterona en el organismo o, a veces, por un exceso de otro tipo de esteroides. Un tumor pequeño de las glándulas suprarrenales segrega a veces cantidades de aldosterona, una afeccion que se conoce como <>. La aldosterona aumenta la velocidad de reabsorción de sal y agua en los tubulos renales, con lo que disminuye la perdida de estas sustancias por orina al mismo tiempo que se provoca el aumento de volumen de sangre y de liquido extracelular. En consecuencia se produce hipertensión.
EL SISTEMA RENINA-ANGIOTENSINA: SU FUNCIÓN EN EL CONTROL DE LA PRESIÓN ARTERIAL.
Además de la capacidad de los riñones de controlar la presión arterial a través de los cambios de volumen del liquido extracelular, los riñones también tienen otro mecanismo potente para controlar la presión arterial: el sistema renina-angiotensina.
La renina es una enzima proteica liberada por los riñones cuando la presión arterial desciende demasiado. A su vez, eleva la presión arterial de varias formas, con lo que ayuda a corregir el descenso inicial de la presión.
COMPONENTES DEL SISTEMA RENINA-ANGIOTENSINA.
La renina se sintetiza y almacena en una forma inactiva conocida como prorrenina en las células yuxtaglomerulares (células YG) de los riñones. Las células YG son miocitos lisos modificados situados principalmente en las paredes de las arteriolas aferentes, inmediatamente proximales a los glomérulos. Cuando desciende la presión arterial se producen una serie de reacciones intrínsecas de los riñones que provocan la escisión de muchas de las moléculas de prorrenina de las células YG y la liberación de renina, la mayor parte de la cual entra en la circulación sanguínea renal para circular después por todo el organismo.
La renina actua enzimáticamente sobre otra proteína plasmática, una globulina denominada sustrato de renina (o angiotensinógeno), para liberar un péptido de 10 aminoacidos, la angiotensina I.
Unos segundos o minutos después de la formación de angiotensina I se escinden otros dos aminoácidos a partir de la angiotensina I para formar el péptido de ocho aminoácidos angiotensina II. Otros tejidos, como los riñones y los vasos sanguíneos, también contienen enzima convertidora y, por tanto, forman angiotensina II localmente.
LA ANGIOTENSINA II PROVOCA RETENCIÓN RENAL DE SAL Y AGUA: UN MEDIO IMPORTANTE PARA EL CONTROL A LARGO PLAZO DE LA PRESIÓN ARTERIAL.
La angiotensina II hace que los riñones retengan sal y agua de dos formas principales:
1) La angiotensina II actúa directamente solo en los riñones para provocar la retención de sal y agua.
2) La angiotensina II provoca la secreción de aldosterona de las glándulas suprarrenales; la aldosterona, a su vez, aumenta la reabsorción de sal y agua en los túbulos renales.
MECANISMOS DE LOS EFECTOS RENALES DIRECTOS DE LA ANGIOTENSINA II QUE PROVOCAN LA RETENCIÓN DE SAL Y AGUA.
La angiotensina tiene varios efectos renales directos que hacen que los riñones retengan sal y agua. Uno de los efectos principales es contraer las arteriolas renales, con lo que disminuye el flujo sanguíneo a través de los riñones.
LA ANGIOTENSINA II AUMENTA LA RETENCIÓN DE SAL Y AGUA EN LOS RIÑONES AL ESTIMULAR LA ALDOSTERONA.
La angiotensina II también es uno de los factores estimulantes mas potentes de la secreción de aldosterona por las glándulas suprarrenales. Por tanto, la velocidad de secreción de aldosterona aumenta también cuando se activa el sistema renina-angiotensina.
Una de las funciones consecuentes de la aldosterona consiste en lograr un aumento importante de la reabsorción de sodio en los túbulos renales, con lo que aumenta el sodio en el liquido extracelular.
FUNCION DEL SISTEMA RENINA-ANGIOTENSINA EN EL MANTENIMIENTO DE UNA PRESIÓN ARTERIAL NORMAL A PESAR DE LAS GRANDES VARIACIONES DE LA INGESTIÓN DE SAL.
Una de las funciones mas importantes del sistema renina-angiotensina es permitir que la persona ingiera cantidades muy pequeñas o muy grandes de sal sin provocar grandes cambios del volumen del líquido extracelular ni de la presión arterial. Después, el aumento de la presión arterial aumenta a su vez el flujo sanguíneo a través de los riñones, además de otros efectos, lo que reduce la velocidad de secreción de renina hasta un nivel muy inferior y consigue secuencialmente disminuir la retención renal de sal y agua, devolviendo el volumen de líquido extracelular casi hasta la normalidad y, por ultimo, devolviendo la propia presión arterial también casi hasta la normalidad.
TIPOS DE HIPERTENSION EN QUE INTERVIENE LA ANGIOTENSINA: HIPERTENSIÓN PROVOCADA POR UN TUMOR SECRETOR DE RENINA O POR ISQUEMIA RENAL.
En ocasiones aparece un tumor de células YG que segrega cantidades enormes de renina; a su vez, se forman cantidades igualmente enormes de angiotensina II. En todos los pacientes en los que se ha dado de este fenómeno se ha desarrollado una hipertensión importante.
HIPERTENSIÓN DE GOLDBLATT CON RIÑÓN ÚNICO.
Cuando se elimina un riñón y se coloca un elemento constrictor en la arteria renal del riñón remanente, el efecto inmediato es un gran descenso de la presión en la arteria renal distalmente al elemento constrictor. Después, en segundos o minutos, la presión arterial sistémica comienza a aumentar, y sigue haciéndolo durante varios días. Lo habitual es que la presión aumente con rapidez en la primera hora, mas o menos, y este efecto se sigue de un aumento adicional mas lento a lo largo de varios días.
HIPERTENSIÓN DE GOLDBLATT CON DOS RIÑONES.
La hipertensión también puede aparecer cuando se produce la constricción solo de un riñón, mientras que la arteria del otro es normal. El riñón que tiene la constriccion segrega renina y también retiene sal y agua por el descenso de la presión de la renina producida por el riñón isquémico. Esta renina provoca la formación de angiotensina II y aldosterona, circulando ambas hacia el riñón contrario haciendo que retenga sal y agua. Es decir, ambos riñones retienen sal y agua, pero por motivos diferentes. En consecuencia, se desarrolla hipertensión.
HIPERTENSIÓN CAUSADA POR RIÑONES ENFERMOS QUE SEGREGAN RENINA CRÓNICAMENTE.
A menudo hay zonas parcheadas enfermas en uno o ambos riñones, que se vuelven isquémicos por la constricción vascular local o infartos, mientras que otras áreas de los riñones son normales. Cuando se produce esta situación, se consiguen efectos casi idénticos a los de la hipertensión de Goldblatt con dos riñones.
HIPERTENSION PRIMARIA (ESENCIAL)
Parece que el 90-95 % de todas las personas que tienen hipertensión tienen <>, también conocida como <> por muchos médicos. Estos términos significan, simplemente, que la hipertensión es de origen desconocido, al contrario que las formas de hipertensión son secundarias a causas conocidas, como la estenosis de la arteria renal o formas monogénicas de hipertensión.
En la mayoría de los pacientes el aumento excesivo de peso y la vida sedentaria parecen desempeñar un papel importante en la causa de la hipertensión. La mayoría de los pacientes hipertensos tienen sobrepeso y en los estudios de distintas poblaciones parece demostrarse que un aumento excesivo de peso y la obesidad explican hasta el 65-75% del riesgo de desarrollar hipertensión primaria.
ANALISIS GRAFICO DE CONTROL DE LA PRESION ARTERIAL EN LA HIPERTENSIÓN ESENCIAL.
Se muestra un análisis grafico de le hipertensión esencial. Las curvas de esta figura se conocen como curvas de función renal con sobrecarga de sodio porque, en cada caso, la presión arterial aumenta muy lentamente durante muchos días o semanas mediante el incremento gradual de la ingestión de sodio. La curva de tipo carga de sodio puede determinarse aumentando la ingestión de sodio a un nuevo nivel cada pocos días, y esperando después a que la eliminación renal de sodio entre en equilibrio con la ingestión, registrando al mismo tiempo los cambios de la presión arterial.
TRATAMIENTO DE LA HIPERTENSION ESENCIAL
En las normas actuales de tratamiento de la hipertensión se recomienda, como primer paso, modificar el estilo de vida con el objetivo de aumentar la actividad física y la perdida de peso en la mayoría de los casos. Para tratar la hipertensión se usan dos clases generales de fármacos: 1) fármacos vasodilatadores, que aumentan el flujo sanguíneo renal y la velocidad de filtración glomerular, y 2) fármacos natriuréticos o diuréticos, que disminuyen la reabsorción tubular de sal y agua.
RESUMEN DEL SISTEMA CON MÚLTIPLES ASPECTOS INTEGRADOS DE REGULACIÓN DE LA PRESIÓN ARTERIAL.
Hasta la fecha esta claro que la presión arterial esta regulada no por un sistema sencillo de control, sino por varios sistemas interrelacionados, cada uno de los cuales realiza una función especifica. Por ejemplo, cuando una persona tiene una hemorragia tan importante que la presión cae súbitamente, el sistema de control de la presión debe reponerse inmediatamente a un nivel suficientemente alto para que la persona pueda vivir superando el episodio agudo. El segundo es devolver el volumen de sangre y la presión arterial a sus valores normales, de forma que el sistema circulatorio pueda restablecer la normalidad completa y no solo recuperando los niveles necesarios para la supervivencia.
MECANISMOS A LARGO PLAZO PARA LA REGULACIÓN DE LA PRESIÓN ARTERIAL.
Aunque algunas veces se desarrolla un mecanismo de retroalimentación positiva para el control de la presión arterial que se hace casi infinita, lo que significa que la presión podría volver casi totalmente a la normalidad, y no parcialmente, hasta la presión que consigue una eliminación normal de sal y agua en los riñones.
Especialmente importante es la interaccion del sistema renina-angiotensina con los mecanismos de aldosterona y liquidos renales. Por ejemplo, la ingestión de sal de una persona es muy variable de un dia a otro. De este modo, el control de la presión arterial comienza siempre con cambios en el estilo de vida relacionados con el control nervioso de la presión y después continua con el mantenimiento de las características de control intermedio de la presión para por ultimo, estabilizar la presión a lo largo plazo utilizando el mecanismo de control de liquidos renal-corporal.
Brandon vazquez balanzar
Gasto cardíaco, retorno venoso y su regulaciónEl gasto cardíaco es la cantidad de sangre que bombea el corazón hacia la aorta cada minuto. También es la cantidad de sangre que fluye por la circulación y uno de los factores más importantes que deben tenerse en cuenta en relación con la circulación, ya que es la suma de los flujos sanguíneos de todos los tejidos del organismo. El retorno venoso es la cantidad del flujo sanguíneo que vuelve desde las venas hacia la aurícula derecha por minuto. El retorno venoso y el gasto cardíaco deben ser iguales entre sí, excepto durante algunos latidos cardíacos que se producen cuando la sangre se almacena o elimina temporalmente del corazón y los pulmones. Valores normales del gasto cardíaco en reposo y durante la actividad
Valores normales del gasto cardíaco en reposo y durante la actividad
El gasto cardíaco varía mucho con el nivel de actividad del organismo. Entre otros, los factores siguientes afectan directamente al gasto cardíaco:
1) El nivel básico del metabolismo del organismo; 2) el ejercicio físico; 3) la edad, y 4) el tamaño del organismo. En los hombres jóvenes y sanos el gasto cardíaco medio en reposo alcanza los 5,6 l/min y los 4,9 l/min en las mujeres. Cuando también se tiene en cuenta el factor de la edad, se dice que el gasto
cardíaco medio de un adulto en reposo es casi 5 l/min en números redondos, ya que la actividad corporal y la masa de algunos tejidos (p. ej., el músculo esquelético) disminuyen cuando aumenta la edad.Índice cardíaco
En estudios experimentales se ha demostrado que el gasto cardíaco aumenta en proporción a la superficie corporal. En consecuencia, el gasto cardíaco se expresa en términos de índice cardíaco, que es el gasto cardíaco por metro cuadrado de superficie corporal. Una persona media que pesa
70 kg tiene una superficie corporal en torno a 1,7 m2, lo que significa que el índice cardíaco medio normal de los adultos es de 3 l/min/m2 de superficie corporal. Efecto de la edad en el gasto cardíacoA los 10 años aumenta rápidamente por encima de los 4 l/min/m2 y disminuye hasta los 2,4 l/min/m2 a los 80 años. En este capítulo se explica más adelante que el gasto cardíaco está regulado a lo largo de la vida en proporción directa a la actividad metabólica total. Por tanto, el descenso del índice
Efecto de la edad en el gasto cardíacoA los 10 años aumenta rápidamente por encima de los 4 l/min/m2 y disminuye hasta los 2,4 l/min/m2 a los 80 años. En este capítulo se explica más adelante que el gasto cardíaco está regulado a lo largo de la vida en proporción directa a la actividad metabólica total. Por tanto, el descenso del índice
cardíaco indica el descenso de la actividad o de la masa muscular con la edad.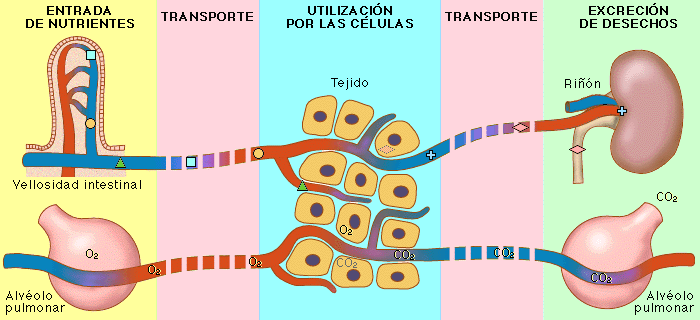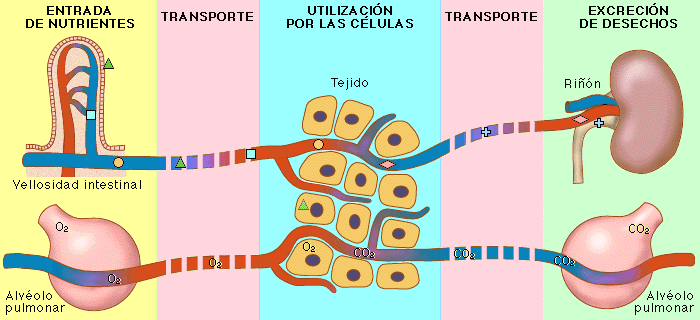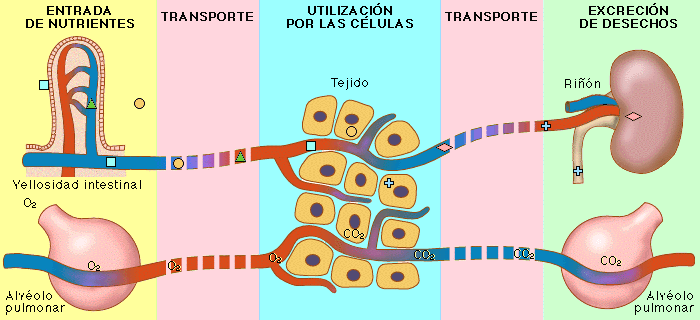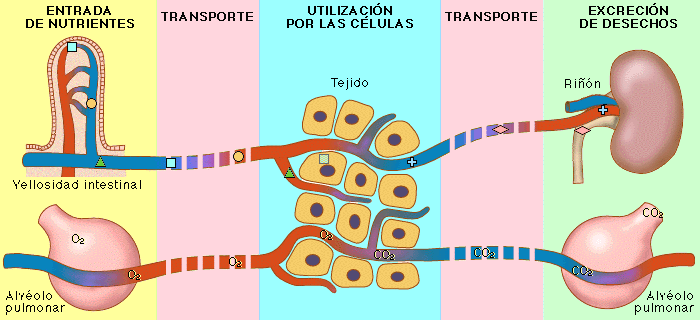 Control del gasto cardíaco por el retorno venoso: mecanismo de Frank-Starling del corazón
Control del gasto cardíaco por el retorno venoso: mecanismo de Frank-Starling del corazón
Cuando se afirma que el gasto cardíaco está controlado por el retorno venoso, quiere decirse que no es el corazón propiamente el que, por lo general, controla el gasto cardíaco, sino que hay otros factores de la circulación periférica que afectan al flujo de sangre hacia el corazón desde las venas, lo que se conoce como retorno venoso, que actúan como controladores principales. La razón principal por la que los factores periféricos son tan importantes en el control de gasto cardíaco es que el corazón tiene un mecanismo propio que le permite bombear automáticamente, sin tener en cuenta la cantidad de sangre que entre en la aurícula derecha desde las venas. Este mecanismo se conoce como ley de Frank-Starling del corazón.Básicamente, en esta ley se afirma que cuando aumenta la cantidad de flujo sanguíneo hacia el corazón se produce un estiramiento de las paredes de las cámaras cardíacas. Como consecuencia del estiramiento el músculo cardíaco se contrae con una fuerza mayor, y esta acción vacía el exceso de sangre que ha entrado desde la circulación sistémica. Por tanto, la sangre que fluye hacia el corazón es bombeada sin retraso hacia la aorta y fluye de nuevo a través de la circulación. Otro factor importante, es que el estiramiento del corazón hace que se bombee más deprisa, lo que da lugar a una frecuencia cardíaca mayor, es decir, el estiramiento del nódulo sinusal de la pared de la aurícula derecha tiene un efecto directo sobre el ritmo del propio nódulo, aumentando la frecuencia cardíaca hasta en un 10-15%. Además, el estiramiento de la aurícula derecha inicia un reflejo nervioso, conocido como reflejo Bainbridge, llega primero al centro vasomotor del cerebro y después vuelve al corazón a través de los nervios simpáticos y los vagos, aumentando también la frecuencia cardíaca.
En la mayoría de las situaciones que no causan estrés el gasto cardíaco se controla principalmente por factores periféricos que determinan el retorno venoso. No obstante, como expondremos más adelante en este capítulo, el corazón se convierte en el factor limitante que determina el gasto
cardíaco cuando el retorno sanguíneo es mayor que el que puede bombear el corazón. El gasto cardíaco es la suma de los flujos sanguíneos en
El gasto cardíaco es la suma de los flujos sanguíneos en
todos los tejidos: el metabolismo tisular regula la mayor parte del flujo sanguíneo local
El retorno venoso hacia el corazón es la suma de todo el flujo sanguíneo local a través de todos los segmentos tisulares de la circulación periférica. Por tanto, se deduce que la regulación del gasto cardíaco es la suma de todos los mecanismos reguladores del flujo sanguíneo local.Los mecanismos de regulación del flujo sanguíneo local se comentaron en el tema. En la mayoría de los tejidos el flujo sanguíneo lo hace principalmente en proporción al metabolismo de cada tejido. Por ejemplo, el flujo sanguíneo local casi siempre aumenta cuando lo hace el consumo tisular de oxígeno.Obsérvese que cuando aumenta el trabajo cardíaco durante el ejercicio, también aumentan
paralelamente el consumo de oxígeno y el gasto cardíaco.El corazón tiene límites en el gasto cardíaco que puede
alcanzar
La cantidad de sangre que el corazón puede bombear tiene unos límites definidos, que pueden expresarse cuantitativamente en forma de curvas de gasto cardíaco. Obsérvese que el nivel de la meseta de esta curva de
gasto cardíaco normal es de 13 l/min, 2,5 veces el gasto cardíaco normal de 5 l/min, lo que significa que el corazón de un ser humano normal que actúe sin una estimulación especial puede bombear un retorno venoso hasta 2,5 veces el retorno venoso normal antes de que el corazón se convierta en el
factor limitante en el control del gasto cardíaco.
Factores que provocan un corazón hipereficazHay dos tipos de factores que hacen que el corazón bombee mejor de lo normal: 1) la estimulación nerviosa, y 2) la hipertrofia del músculo cardíaco.Factores que provocan un corazón hipoeficaz
Cualquier factor que disminuya la capacidad del corazón de bombear la sangre provoca la hipoeficacia. Algunos de los factores que pueden reducir la capacidad de bombeo del corazón son los siguientes:
• Aumento de la presión arterial contra la cual debe bombear el corazón, como en la hipertensión grave.
• Inhibición de la excitación nerviosa del corazón.
• Factores patológicos que provocan alteraciones del ritmo cardíaco o de la frecuencia cardíaca.
• Bloqueo de una arteria coronaria, para provocar un «ataque cardíaco».
• Cardiopatía valvular.
• Cardiopatía congénita.
• Miocarditis, una inflamación del músculo cardíaco.• Hipoxia cardíacaEfecto del sistema nervioso para aumentar la presión arterial durante el ejercicio
Durante el ejercicio, el aumento intenso del metabolismo en los músculos esqueléticos activos actúa directamente en las arteriolas musculares para relajarlos y permitir el acceso adecuado del oxígeno y otros nutrientes necesarios para mantener la contracción muscular. Evidentemente, así se produce un descenso importante de la resistencia periférica total, lo que normalmente también disminuiría la presión arterial. No obstante, el sistema nervioso lo compensa inmediatamente.
La misma actividad cerebral que envía las señales motoras a los músculos envía señales simultáneamente a los centros nerviosos autónomos del cerebro para provocar la actividad circulatoria, provocando la constricción de las venas grandes y el aumento de la frecuencia y de la contractilidad del corazón. Todos estos cambios actúan en conjunto aumentando la presión arterial por encima de lo normal, lo que a su vez empuja aún más flujo sanguíneo a través de los músculos activos.
En resumen, el sistema nervioso tiene un papel clave para prevenir la caída de la presión arterial hasta niveles desastrosos cuando los vasos sanguíneos tisulares se dilatan y el retorno venoso y el gasto cardíaco aumentan por encima de lo normal. De hecho, durante el ejercicio, el sistema nervioso va incluso más allá, proporcionando otras señales que elevan la presión arterial por encima de lo normal, lo que sirve para aumentar el gasto cardíaco otro 30-100%.Elevación y disminución patológica del gasto cardíaco
En los seres humanos sanos el gasto cardíaco medio se mantiene sorprendentemente constante de una persona a otra. No obstante, hay muchas anomalías clínicas que aumentan o disminuyen el gasto cardíaco.Elevación del gasto cardíaco provocada por una reducción de la resistencia periférica totalUna de las características distintivas de esas situaciones es que todas son el resultado de la reducción crónica de la resistencia periférica total y ninguna es consecuencia de una excitación excesiva del propio corazón, como explicaremos más adelante. Revisaremos algunas de las situaciones que disminuyen la resistencia periférica y, al mismo tiempo, aumentan el gasto cardíaco por encima de lo normal.
1. Beriberi. Esta enfermedad está provocada por una cantidad insuficiente de la vitamina tiamina (vitamina B1) en la dieta. La falta de esta vitamina disminuye la capacidad de los tejidos de usar algunos nutrientes celulares y mecanismos del flujo sanguíneo tisular local que, a su vez, provoquen una vasodilatación periférica compensadora. En ocasiones, la resistencia periférica total disminuye hasta tan solo la mitad de lo normal, por lo que los niveles de retorno venoso y gasto cardíaco a largo plazo también aumentan hasta el doble de lo normal.
2. Fístula (cortocircuito) arteriovenosa (AV). Ya hemos hablado de que cada vez que se crea una fístula (también denominada cortocircuito AV) entre una arteria y una vena importantes pasa una gran cantidad de flujo sanguíneo directamente desde la arteria hacia la vena, lo cual, además, disminuye en gran medida la resistencia periférica total y, asimismo, aumenta el retorno venoso y
el gasto cardíaco.
3. Hipertiroidismo. En el hipertiroidismo, el metabolismo de la mayoría de los tejidos del organismo está muy aumentado y la utilización de oxígeno aumenta, liberándose productos vasodilatadores desde los tejidos. Por tanto, la resistencia periférica total disminuye mucho porque el control del flujo sanguíneo tisular local reacciona por todo el cuerpo; en consecuencia, el retorno venoso y el gasto cardíaco aumentan hasta el 40-80% por encima de lo normal.4. Anemia. En la anemia se producen dos efectos periféricos que disminuyen en gran medida la resistencia periférica total. Uno de estos efectos es la disminución de la viscosidad de la sangre, como consecuencia del descenso de la concentración de eritrocitos. El otro es un menor aporte de oxígeno a los tejidos, lo que provoca la vasodilatación local. En consecuencia, el gasto cardíaco aumenta mucho. Cualquier otro factor que disminuya la resistencia periférica total crónicamente también aumentará el gasto cardíaco si la presión arterial no disminuye demasiado.Descenso del gasto cardíaco provocado por factores periféricos no cardíacos: descenso del retorno venoso
Cualquier factor que interfiera con el retorno venoso también provoca el descenso del gasto cardíaco. Algunos de estos factores son los siguientes:1. Descenso del volumen de sangre. Con mucho, el factor periférico no cardíaco más frecuente que provoca el descenso del gasto cardíaco es la reducción del volumen de sangre, a menudo debido a una hemorragia. La pérdida de sangre disminuye el llenado del aparato vascular hasta un nivel tan bajo que no hay sangre suficiente en los vasos sanguíneos periféricos para generar presiones vasculares periféricas suficientes para empujar la sangre de vuelta hacia el corazón.
2. Dilatación venosa aguda. La dilatación venosa aguda se produce a menudo cuando el sistema nervioso simpático se vuelve súbitamente inactivo. Por ejemplo, un desvanecimiento es consecuencia frecuente de una pérdida súbita de actividad del sistema nervioso simpático que provoca una dilatación muy importante de los vasos periféricos de capacitancia, en especial de las
venas. Esta dilatación disminuye la presión de llenado en el aparato vascular, ya que el volumen de sangre no puede crear la presión adecuada en unos vasos sanguíneos periféricos que ahora están flácidos. En consecuencia, la sangre «se asienta» en los vasos y no vuelve hacia el corazón con la
rapidez normal.
3. Obstrucción de las grandes venas. En casos aislados las grandes venas que llegan al corazón se obstruyen, y la sangre de los vasos periféricos no puede volver al corazón. En consecuencia, se produce un descenso importante del gasto cardíaco.
4. Reducción de la masa tisular, en especial de la masa de músculo esquelético. En caso de envejecimiento normal o de períodos prolongados de inactividad física se produce normalmente una reducción del tamaño de los músculos esqueléticos. A su vez, esta reducción disminuye el consumo total de oxígeno y las necesidades de flujo sanguíneo de los músculos, con lo que
disminuye el flujo sanguíneo en el músculo esquelético y el gasto cardíaco.
5. Reducción del ritmo metabólico de los tejidos. Si se reduce el ritmo metabólico, como sucede en el músculo esquelético durante un reposo en cama prolongado, el consumo de oxígeno y las necesidades de nutrición de los tejidos también disminuirán. En consecuencia, disminuye el flujo sanguíneo en los tejidos, con el resultado de un menor gasto cardíaco. Otros trastornos, como el hipotiroidismo, pueden reducir asimismo el ritmo metabólico y, por tanto, el flujo sanguíneo y el gasto cardíaco.Un análisis más cuantitativo de la regulación del gasto
cardíaco
El comentario sobre la regulación del gasto cardíaco que hemos realizado hasta ahora es adecuado para entender los factores que controlan el gasto cardíaco en las situaciones más sencillas. Sin embargo, para entender la regulación del gasto cardíaco en situaciones estresantes especiales, como el ejercicio extremo, la insuficiencia cardíaca y el shock circulatorio, en las secciones siguientes se muestra un análisis cuantitativo más complejo.
Para realizar ese análisis cuantitativo más detallado es necesario distinguir por separado entre los dos factores principales implicados en la regulación del gasto cardíaco: 1) la capacidad de bomba del corazón, representada por las curvas de gasto cardíaco, y 2) los factores periféricos que afectan al flujo de sangre desde las venas al corazón, representados por las curvas de retorno venoso. Después, se pueden unir ambas curvas en un análisis cuantitativo para demostrar cómo interaccionan entre sí para determinar al mismo tiempo el gasto cardíaco, el retorno venoso y la presión en la aurícula
derecha.Curvas de retorno venoso
Antes de realizar un análisis total de la regulación cardíaca tenemos que valorar toda la circulación sistémica, para lo cual primero retiramos el corazón y los pulmones de la circulación de un animal y los reemplazamos con unos sistemas de bomba y de un oxigenador artificial y después se alteran distintos factores, como el volumen de sangre, las resistencias vasculares y la presión venosa central en la aurícula derecha, para determinar cómo actúa la circulación sistémica en distintos estados circulatorios.
En estos estudios se encuentran los tres factores principales siguientes que afectan al retorno venoso hacia el corazón desde la circulación sistémica:
1. Presión en la aurícula derecha, que ejerce una fuerza retrógrada sobre las venas para impulsar el flujo de sangre desde las venas hacia la aurícula derecha.2. Grado de llenado de la circulación sistémica (medido por la presión media del llenado sistémico), que obliga a la sangre sistémica a volver hacia el corazón (esta es la presión medida en cualquier parte de la circulación sistémica cuando se interrumpe todo el flujo de sangre, como se comenta en
detalle más adelante en este capítulo).
3. Resistencia al flujo sanguíneo entre los vasos periféricos y la aurícula derecha. Estos factores se expresan cuantitativamente en la curva de retorno venoso, como explicamos en las secciones siguientes.Métodos para medir el gasto cardíaco
En los experimentos con animales se puede canular la aorta, la arteria pulmonar o las grandes venas que entran en el corazón y medir el gasto cardíaco utilizando un flujómetro. También se puede colocar un flujómetro electromagnético o ultrasónico en la aorta o en la arteria pulmonar para medir
el gasto cardíaco. En el ser humano, el gasto cardíaco se mide por métodos indirectos que no requieren cirugía, excepto en algunos casos aislados. Dos de los métodos que se han usado para estudios experimentales son el método de oxígeno de Fick y el método de dilución del indicador. El gasto cardíaco puede estimarse también mediante ecocardiografía, un método que utiliza ondas
de ultrasonidos desde un transductor colocado sobre la pared torácica o introducido en el esófago del paciente para medir el tamaño de las cámaras cardíacas, así como la velocidad de la sangre que circula desde el ventrículo izquierdo a la aorta. El volumen del impulso se calcula a partir de la
velocidad de la sangre que circula en la aorta y del área en sección transversal de la aorta determinada a partir del diámetro de la aorta que se mide mediante estudio de imagen ecográfico. A continuación se calcula el gasto cardíaco como el producto de este volumen por la frecuencia cardíaca.
Brandon nazario vazquez balanzar 1-B
Regulación nerviosa de la circulación y control rápido de la presión arterialRegulación nerviosa de la circulación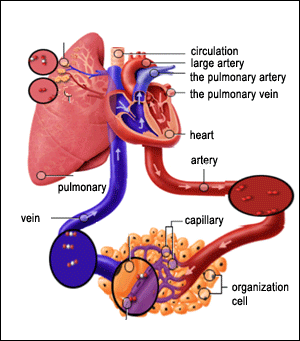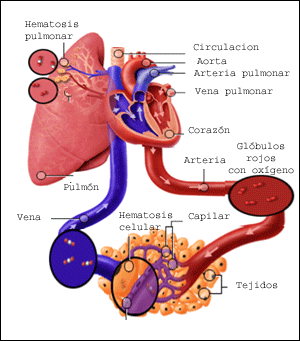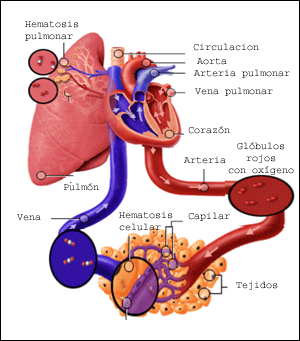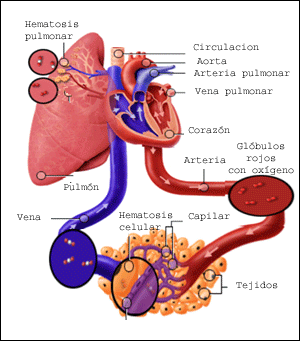 Como hemos comentado en el, el ajuste del flujo sanguíneo en los tejidos y los órganos del cuerpo es principalmente una función de los mecanismos de control en los tejidos locales. En este capítulo veremos cómo el control nervioso de la circulación tiene más funciones globales, como la
Como hemos comentado en el, el ajuste del flujo sanguíneo en los tejidos y los órganos del cuerpo es principalmente una función de los mecanismos de control en los tejidos locales. En este capítulo veremos cómo el control nervioso de la circulación tiene más funciones globales, como la
redistribución del flujo sanguíneo hacia las distintas zonas del organismo, el aumento o descenso de la actividad de bomba cardíaca y el control rápido de la presión arterial sistémica.El sistema nervioso controla la circulación casi totalmente a través del sistema nervioso autónomo. En el presente capítulo consideraremos las características anatómicas y funcionales específicas adicionales.
Sistema nervioso autónomo
Con diferencia, la parte más importante del sistema nervioso autónomo para la regulación de la circulación es el sistema nervioso simpático. No obstante, el sistema nervioso parasimpático contribuye de manera importante a la regulación de la función cardíaca, como se describe más
adelante en este mismo capítulo.
Sistema nervioso simpático
Las fibras nerviosas vasomotoras salen de la médula espinal a través de los nervios de la columna torácica y de los primeros uno o dos nervios lumbares. A continuación, pasan inmediatamente hacia las cadenas simpáticas, cada una de las cuales recorre cada lado de la columna vertebral. Después, siguen dos
rutas hacia la circulación: 1) a través de los nervios simpáticos específicos que inervan principalmente la vasculatura de las vísceras internas y del corazón, entrando casi inmediatamente en las porciones periféricas de los nervios
espinales que se distribuyen hacia la vasculatura de las zonas periféricas. Las vías precisas que siguen esas fibras en la médula espinal y en las cadenas simpáticas.Inervación simpática de los vasos sanguíneos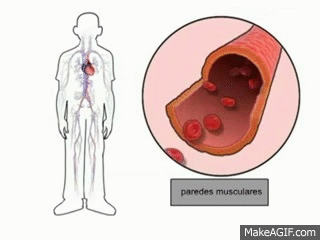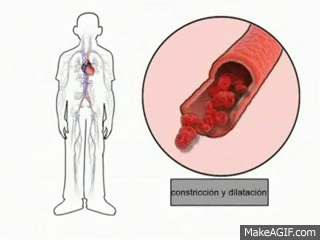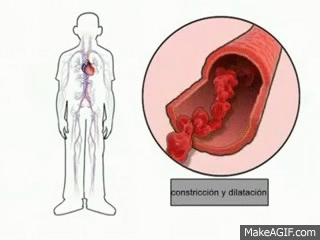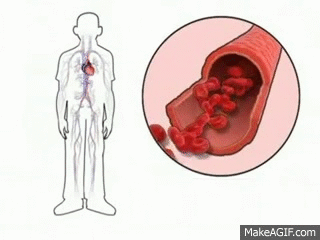 Se muestra la distribución de las fibras nerviosas simpáticas hacia los vasos sanguíneos, demostrándose que en la mayoría de los tejidos están inervados todos los vasos, excepto los capilares. Los esfínteres precapilares y las metaarteriolas están inervados en algunos tejidos como los vasos sanguíneos mesentéricos, aunque normalmente su inervación simpática no es tan densa como en las pequeñas arterias, las arteriolas y las venas.
Se muestra la distribución de las fibras nerviosas simpáticas hacia los vasos sanguíneos, demostrándose que en la mayoría de los tejidos están inervados todos los vasos, excepto los capilares. Los esfínteres precapilares y las metaarteriolas están inervados en algunos tejidos como los vasos sanguíneos mesentéricos, aunque normalmente su inervación simpática no es tan densa como en las pequeñas arterias, las arteriolas y las venas.
La inervación de las pequeñas arterias y arteriolas permite que la estimulación simpática aumente la resistencia al flujo sanguíneo y, por tanto, disminuya la velocidad del flujo sanguíneo a través de los tejidos. La inervación de los vasos grandes, en particular de las venas, hace posible que la estimulación simpática disminuya el volumen de estos vasos. Esta disminución del volumen empuja la sangre hacia el corazón y, por tanto, desempeña un papel muy importante en la regulación de la función de bomba cardíaca, como explicaremos más adelante en este y en capítulos sucesivos.
La estimulación simpática aumenta la frecuencia cardíaca y la contractilidad
Las fibras simpáticas también llegan directamente hasta el corazón, Recuérdese que la estimulación simpática aumenta en gran medida la actividad cardíaca, aumentando tanto la frecuencia cardíaca como su fuerza y el volumen
de bombeo.La estimulación parasimpática reduce la frecuencia cardíaca y la contractilidad
Aunque el sistema nervioso parasimpático es muy importante para muchas otras funciones autónomas del organismo, como el control de muchas acciones gastrointestinales, solo tiene una participación pequeña en la regulación de la función vascular en la mayoría de los tejidos. El efecto circulatorio más importante es el control de la frecuencia cardíaca mediante las fibras nerviosas
parasimpáticas hacia el corazón en los nervios vagos, en la línea
discontinua roja que va desde el bulbo raquídeo directamente hasta el corazón.
Lo más importante es que la estimulación parasimpática provoca un marcado descenso de la frecuencia cardíaca y un ligero descenso de la contractilidad del músculo cardíaco.Sistema vasoconstrictor simpático y su control por el sistema nervioso centralLos nervios simpáticos transportan una enorme cantidad de fibras nerviosas vasoconstrictoras y solo algunas fibras vasodilatadoras. Las fibras vasoconstrictoras se distribuyen esencialmente hacia todos los segmentos de la circulación, pero más hacia algunos tejidos que otros. Este efecto vasoconstrictor simpático es especialmente potente en los riñones, intestinos, bazo y piel, pero lo es mucho menos en el músculo esquelético y el cerebro.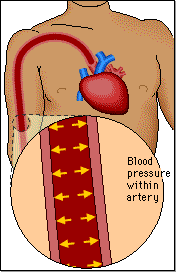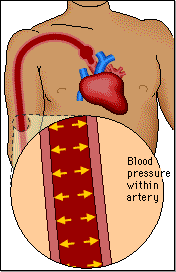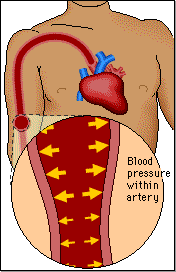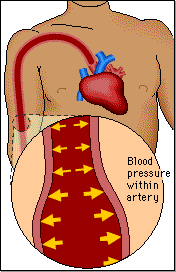 Centro vasomotor del cerebro y control del sistema vasoconstrictor
Centro vasomotor del cerebro y control del sistema vasoconstrictor
Situado bilateralmente en la sustancia reticular del bulbo y en el tercio inferior de la protuberancia, conforma una zona denominada centro vasomotor. Este centro transmite los impulsos parasimpáticos a través de los nervios vagos hacia el corazón y transmite los impulsos simpáticos a través de la médula espinal y los nervios simpáticos periféricos prácticamente hacia todas las arterias, arteriolas y venas del organismo.Aunque la organización total del centro vasomotor aún no se conoce con detalle, en algunos experimentos ha sido posible identificar ciertas zonas importantes en este centro:
1. Una zona vasoconstrictora situada bilateralmente en las porciones anterolaterales de la parte superior del bulbo. Las neuronas que se originan en esta zona distribuyen sus fibras a todos los niveles de la médula espinal, donde excitan las neuronas vasoconstrictoras preganglionares del sistema nervioso simpático.
2. Una zona vasodilatadora situada bilateralmente en las porciones anterolaterales de la mitad inferior del bulbo. Las fibras de estas neuronas se proyectan hacia arriba, hacia la zona vasoconstrictora que acabamos de describir, e inhiben la actividad vasoconstrictora de esta zona, con lo que provocan vasodilatación.
3. Una zona sensitiva situada bilateralmente en el núcleo del tracto solitario de las porciones posterolaterales del bulbo y parte inferior de la protuberancia. Las neuronas de esa zona reciben señales nerviosas sensitivas desde el sistema circulatorio, principalmente a través de los nervios vagos y glosofaríngeos, y emiten señales eferentes desde esta zona sensitiva que facilitan las actividades de control de las zonas tanto vasoconstrictoras como vasodilatadoras, con lo que se consigue el control «reflejo» de muchas funciones circulatorias. Un ejemplo es el reflejo de barorreceptores para controlar la presión arterial, que se describe más adelante en este capítulo.
La constricción parcial continuada de los vasos sanguíneos se debe normalmente al tono vasoconstrictor simpático
En condiciones normales, la zona vasoconstrictora del centro vasomotor transmite señales continuamente hacia las fibras nerviosas vasoconstrictoras simpáticas en todo el cuerpo, provocando descargas lentas de esas fibras a una velocidad entre medio y dos impulsos por segundo. Esta descarga continuada se conoce como tono vasoconstrictor simpático. Estos impulsos mantienen
normalmente un estado parcial de contracción en los vasos sanguíneos, que se conoce como tono vasomotor.Control de la actividad cardíaca por el centro vasomotor
Al mismo tiempo que el centro vasomotor regula la cantidad de constricción vascular, también controla la actividad cardíaca. Las porciones laterales del centro vasomotor transmiten impulsos excitatorios a través de las fibras nerviosas simpáticas hacia el corazón cuando es necesario aumentar
la frecuencia y la contractilidad cardíacas. Por el contrario, cuando es necesario disminuir la función de bomba a la porción medial del centro vasomotor envía señales hacia los núcleos dorsales motores adyacentes de los nervios vagos, que después transmiten los impulsos parasimpáticos a través de los
nervios vagos hacia el corazón para disminuir la frecuencia y la contractilidad cardíacas. Por tanto, el centro vasomotor puede aumentar o disminuir la actividad cardíaca. La frecuencia y la fuerza de la contracción cardíacas aumentan normalmente cuando se produce la vasoconstricción y disminuyen
cuando esta se inhibe.
Función del sistema nervioso en el control rápido de la
presión arterial
Una de las funciones más importantes del control nervioso de la circulación es su capacidad de provocar incrementos rápidos de la presión arterial. Para tal fin, todas las funciones vasoconstrictoras y cardioaceleradoras del sistema nervioso simpático se estimulan a la vez y, al mismo tiempo, se produce una inhibición recíproca de las señales inhibidoras vagales parasimpáticas hacia el corazón. Es decir, se producen tres cambios importantes simultáneamente, cada uno de los cuales aumenta la presión arterial, que son los siguientes:1. La mayoría de las arteriolas de la circulación sistémica se contraen, lo que aumenta mucho la resistencia periférica total y, en consecuencia, la presión arterial.2. Las venas, en especial (aunque también los demás vasos grandes de la circulación), se contraen con fuerza. Esta contracción desplaza la sangre desde los grandes vasos sanguíneos periféricos hacia el corazón, con lo que aumenta el volumen de sangre en las cámaras cardíacas. El estiramiento del corazón provoca entonces un latido más potente de este órgano y, por tanto, el bombeo de mayores cantidades de sangre. Además, aumenta la presión arterial.3. Por último, el sistema nervioso autónomo estimula directamente al corazón, lo que también potencia la bomba cardíaca. Gran parte de este incremento del bombeo cardíaco se debe al aumento de la frecuencia cardíaca, a veces hasta tres veces con respecto a lo normal. Además, las señales nerviosas simpáticas tienen un efecto directo significativo que aumenta la fuerza contráctil del músculo cardíaco, lo cual aumenta la capacidad del corazón de bombear mayores volúmenes de sangre. Durante una estimulación simpática potente el corazón puede bombear aproximadamente dos veces la misma cantidad de sangre que en condiciones normales, lo que contribuye aún más al aumento agudo de la presión arterial.El control nervioso de la presión arterial es rápidoUna característica especialmente importante del control nervioso de la presión arterial es su rapidez de respuesta, comenzando en segundos y aumentando a menudo la presión hasta dos veces con respecto a lo normal en 5-10 s. Por el contrario, la inhibición brusca de la estimulación nerviosa cardiovascular disminuye la presión arterial hasta la mitad de lo normal en 10-40 s, por lo que el control nervioso es, con mucho, el mecanismo más rápido de regulación de la presión arterial.
Mecanismos reflejos para mantener la presión arterial normal
Además de las funciones sobre el ejercicio y el estrés del sistema nervioso autónomo que tienen como objetivo aumentar la presión arterial, hay varios mecanismos de control especial e inconsciente que actúan todo el tiempo para mantener la presión arterial en valores prácticamente normales. Casi todos ellos se basan en mecanismos reflejos de retroalimentación negativa que
describiremos en las secciones siguientes.Sistema de control de la presión arterial mediante
barorreceptores: reflejos barorreceptoresCon mucho, los mecanismos nerviosos mejor conocidos para el control de la presión arterial es el reflejo barorreceptor. Básicamente, este reflejo se inicia en los receptores de estiramiento, conocidos como barorreceptores o presorreceptores, situados en puntos específicos de las paredes de varias
arterias sistémicas de gran tamaño. El aumento de la presión arterial estira los barorreceptores y hace que transmitan las señales hacia el SNC. Las señales de «retroalimentación» vuelven después a través del sistema nervioso autónomo hacia la circulación para reducir la presión arterial hasta el nivel
normal.Reflejo circulatorio iniciado por los barorreceptoresDespués de que las señales de los barorreceptores entren en el núcleo del tracto solitario del bulbo, las señales secundarias inhiben el centro vasoconstrictor del bulbo y excitan el centro parasimpático vagal. Los efectos netos son dos:
1) La vasodilatación de las venas y arteriolas en todo el sistema
circulatorio periférico.
2) el descenso de la frecuencia cardíaca y de la fuerza de contracción cardíaca. Por tanto, la excitación de los barorreceptores por una presión elevada en las arterias provoca el descenso reflejo de la presión arterial como consecuencia tanto del descenso de la resistencia periférica como del gasto cardíaco. Por el contrario, una presión baja tiene los efectos
contrarios, provocando el aumento reflejo de la presión hasta la normalidad.Los barorreceptores atenúan los cambios de la presión arterial durante los cambios de postura del cuerpo
La capacidad de los barorreceptores de mantener una presión arterial relativamente constante en la parte superior del cuerpo es importante cuando una persona se levanta después de haber estado tumbada. Inmediatamente la presión arterial de la cabeza y parte superior del cuerpo tiende a caer y el
descenso importante de esta presión podría provocar la pérdida de conciencia, aunque el descenso de la presión en los barorreceptores provoca un reflejo inmediato que da lugar a una descarga simpática potente en todo el cuerpo, lo que minimiza el descenso de la presión en la cabeza y la parte superior
del cuerpo.
Función «amortiguadora» de la presión del sistema de control de barorreceptores
Como el sistema de barorreceptores se opone tanto al aumento como al descenso de la presión arterial, se denomina sistema amortiguador de la presión y los nervios de los barorreceptores se
conocen como nervios amortiguadores.Control de la presión arterial por los quimiorreceptores carotídeos y aórticos: efecto del bajo nivel de oxígeno sobre la presión arterialEstrechamente asociado al control de los barorreceptores del sistema de presión actúa un reflejo de quimiorreceptores que funciona de una forma muy similar al reflejo de barorreceptores, excepto porque son los quimiorreceptores, y no los receptores de estiramiento, los que inician la respuesta.
Los quimiorreceptores están formados por células quimiosensibles al bajo nivel de oxígeno, al exceso de dióxido de carbono y al exceso de iones hidrógeno. Se localizan en varios órganos quimiorreceptores pequeños, con un tamaño de unos 2 mm (dos cuerpos carotídeos, cada uno de los
cuales se sitúa en la bifurcación de cada arteria carótida común, y habitualmente entre uno y tres cuerpos aórticos adyacentes a la aorta). Los quimiorreceptores excitan las fibras nerviosas que, junto a las fibras de los barorreceptores, llegan por los nervios de Hering y los nervios vagos hacia el
centro vasomotor del tronco del encéfalo. Cada cuerpo carotídeo o aórtico esta irrigado por un flujo sanguíneo abundante a través de una arteria nutricia pequeña, por lo que los quimiorreceptores siempre están en estrecho contacto con la sangre arterial. Siempre que la presión arterial cae por debajo de un nivel crítico los quimiorreceptores se estimulan porque el descenso del flujo sanguíneo provoca la disminución del oxígeno y también la acumulación excesiva de dióxido de carbono e iones hidrógeno que no se eliminan por una sangre que fluye lentamente.
Las señales transmitidas desde los quimiorreceptores excitan el centro vasomotor, y esta respuesta eleva la presión arterial hasta la normalidad. No obstante, este reflejo de quimiorreceptores no es un controlador potente de la presión arterial hasta que esta cae por debajo de 80 mmHg. Por tanto, este
reflejo adquiere su importancia con las presiones más bajas, ayudando a prevenir aún más descensosadicionales de la presión arterial.Reflejos auriculares y en la arteria pulmonar que regulan la presión arterial
Tanto la aurícula como las arterias pulmonares tienen en sus paredes receptores de estiramiento denominados receptores de baja presión. Estos receptores son similares a los receptores de estiramiento de los barorreceptores que hay en las arterias sistémicas grandes. Estos receptores de baja presión desempeñan un papel importante, en especial al minimizar los cambios de presión
arterial en respuesta a los cambios en el volumen de sangre. Por ejemplo, si se perfunden con rapidez 300 ml de sangre a un perro que tiene todos los receptores intactos, la presión arterial aumenta solo unos 15 mmHg, pero si se denervan los barorreceptores arteriales la presión aumenta en torno a
40 mmHg. Si se denervan también los receptores de baja presión, la presión arterial aumenta hasta unos 100 mmHg.
Es decir, puede verse que aunque los receptores de baja presión en la arteria pulmonar y en la aurícula no puedan detectar la presión arterial sistémica, sí detectan los incrementos simultáneos de la presión en las zonas de baja presión de la circulación provocados por el aumento de volumen, provocando reflejos paralelos a los de los barorreceptores para conseguir que el sistema reflejo
controle con mayor potencia la presión arterial.Respuesta isquémica del sistema nervioso central: control de la presión arterial por el centro vasomotor del cerebro en respuesta a un descenso del flujo sanguíneo cerebral
La mayor parte del control nervioso de la presión sanguínea se logra por los reflejos que se originan en los barorreceptores, los quimiorreceptores y los receptores de presión baja, todos ellos situados en la circulación periférica fuera del cerebro. No obstante, cuando el flujo sanguíneo que se dirige
hacia el centro vasomotor en la parte inferior del tronco del encéfalo disminuye lo suficiente para provocar un defecto nutricional, es decir, para provocar la isquemia cerebral, las neuronas vasoconstrictoras y cardioaceleradoras del centro vasomotor responden directamente a la isquemia y se excitan con fuerza. Cuando se produce esta excitación, la presión arterial sistémica aumenta hasta los niveles máximos que pueda bombear el corazón. Se cree que este efecto se debe al fracaso de la sangre que fluye lentamente y no puede llevarse el dióxido de carbono del centro vasomotor del
tronco del encéfalo. Con niveles bajos de flujo sanguíneo hacia el centro vasomotor, la concentración local de dióxido de carbono aumenta mucho y tiene un efecto muy potente para estimular las zonas de
control vasomotor nervioso simpático en el bulbo raquídeo.
Es posible que haya otros factores, como la acumulación de ácido láctico y de otras sustancias ácidas en el centro vasomotor, que también contribuyen a la importante estimulación y elevación de la presión arterial. Esta elevación en respuesta a una isquemia cerebral se conoce como respuesta
isquémica del SNC.
El efecto isquémico sobre la actividad vasomotora puede elevar drásticamente la presión arterial media, llegando incluso a los 250 mmHg durante hasta 10 min. El grado de vasoconstricción simpática provocado por la isquemia cerebral intensa a menudo es tan grande que algunos de los vasos periféricos se ocluyen total o casi totalmente. Por ejemplo, los riñones interrumpen totalmente su producción de orina por la constricción arteriolar renal en respuesta a la descarga simpática. Por tanto, la respuesta isquémica del SNC es uno de los activadores más potentes de todos los activadores
del sistema vasoconstrictor simpático.Características especiales del control nervioso
de la presión arterial
Función de los nervios y músculos esqueléticos en el
incremento del gasto cardíaco y la presión arterialAunque el control nervioso de la circulación de acción más rápida se efectúa a través del sistema nervioso autónomo, hay al menos dos situaciones en las que los nervios y músculos esqueléticos también tienen un papel importante en las respuestas circulatorias. Reflejo de compresión abdominal Cuando se provoca un reflejo de barorreceptores o quimiorreceptores, las señales nerviosas se transmiten simultáneamente a través de los nervios esqueléticos hacia los músculos esqueléticos del organismo, en particular hacia los músculos abdominales. La contracción muscular comprime todos
los reservorios venosos del abdomen, ayudando a trasladar la sangre desde los reservorios vasculares abdominales hacia el corazón. En consecuencia, el corazón dispone de una mayor cantidad de sangre para bombear. Esta respuesta global se conoce como reflejo de compresión abdominal. El
efecto resultante sobre la circulación es el mismo que el causado por los impulsos vasoconstrictores simpáticos cuando contraen las venas: aumento del gasto cardíaco y aumento de la presión arterial.
Es probable que el reflejo de compresión abdominal sea más importante de lo que se pensaba en el pasado, porque es bien sabido que las personas cuyos músculos esqueléticos se han paralizado son mucho más propensas a sufrir episodios de hipotensión que las personas con músculos esqueléticos
normales.Aumento del gasto cardíaco y de la presión arterial causado por la contracción del músculo esquelético durante el ejercicioCuando los músculos esqueléticos se contraen durante el ejercicio comprimen los vasos sanguíneos por todo el organismo. Incluso la anticipación del ejercicio aprieta los músculos, con lo que se comprimen los vasos musculares y abdominales. Esta compresión traslada sangre desde los vasos periféricos hacia el corazón y los pulmones y, por tanto, aumenta el gasto cardíaco. Este efecto es esencial como ayuda para provocar un incremento del gasto cardíaco en 5-7 veces, como sucede a veces durante el ejercicio intenso. A su vez, el aumento del gasto cardíaco es un componente esencial del incremento de la presión arterial durante el ejercicio, un incremento que suele partir de una media normal de 100 mmHg hasta 130-160 mmHg.Ondas respiratorias en la presión arterialCon cada ciclo de respiración la presión arterial aumenta y cae 4-6 mmHg en forma de oleadas, provocando las ondas respiratorias de la presión arterial. Las ondas son consecuencia de varios efectos, algunos de los cuales tienen un origen reflejo:
1. Muchas de las «señales respiratorias» que surgen en el centro de la respiración del bulbo se «desbordan» hacia el centro vasomotor con cada ciclo respiratorio.2. Cada vez que una persona inspira la presión de la cavidad torácica se vuelve más negativa de lo habitual, provocando la expansión de los vasos sanguíneos torácicos y reduciendo, en consecuencia, la cantidad de sangre que vuelve hacia el corazón izquierdo y disminuyendo momentáneamente el gasto cardíaco y la presión arterial.3. Los cambios de presión provocados en los vasos torácicos por la respiración excitan los receptores de estiramientos vasculares y auriculares.
Aunque es difícil analizar las relaciones exactas de todos estos factores al provocar las ondas de presión respiratorias, el resultado neto durante la respiración normal es un aumento de la presión arterial durante la parte precoz de la espiración y un descenso de la presión durante el resto del ciclo
respiratorio. Durante la respiración profunda la presión sanguínea aumenta y disminuye hasta 20 mmHg con cada ciclo respiratorio.
Brandon nazario vazquez balanzar 1-B
VISIÓN GENERAL DE LA CIRCULACIÓN;BIOFÍSICA DE LA PRESIÓN,EL FLUJO Y LA RESISTENCIA
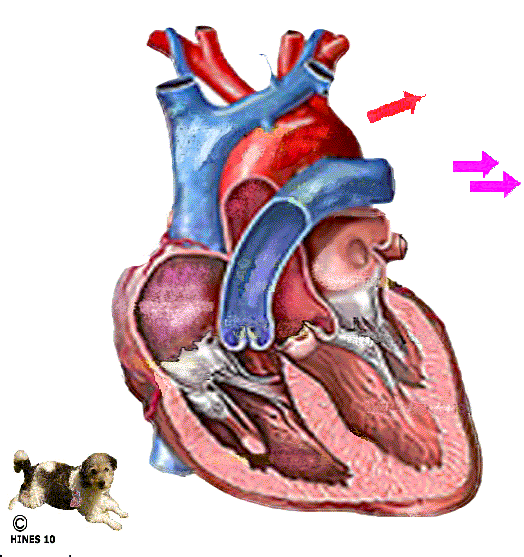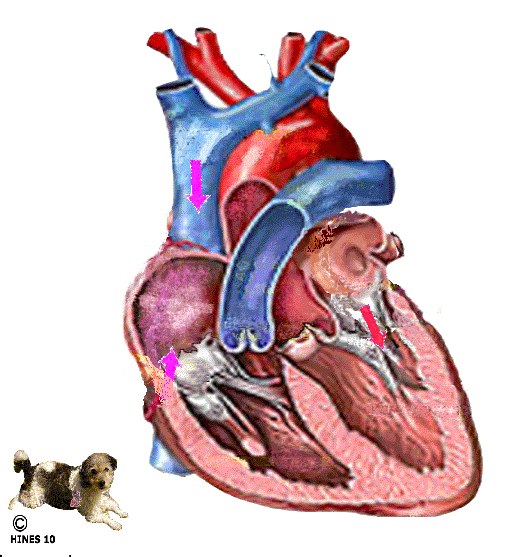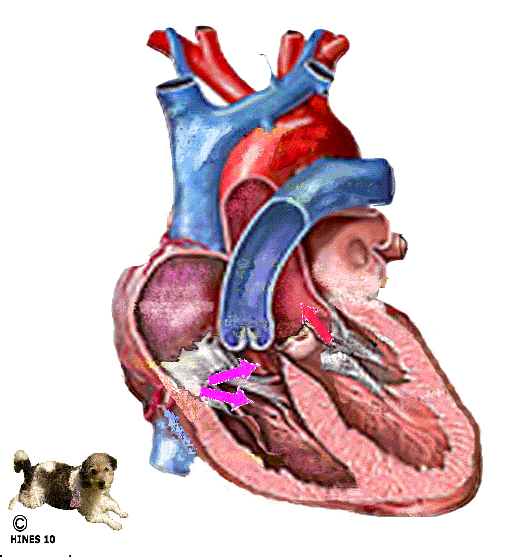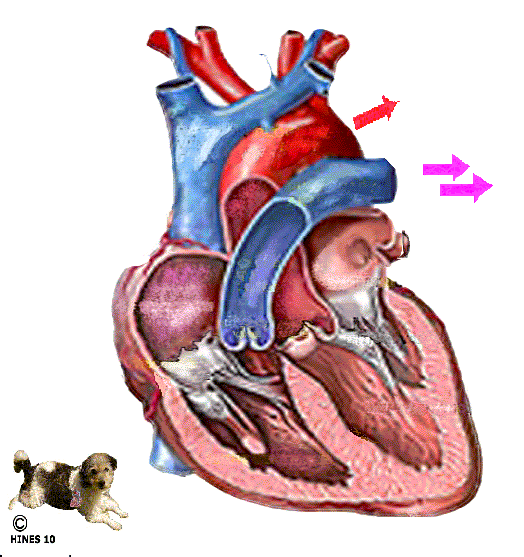
La función de la circulación consiste en atender las necesidades del organismo: transportar nutrientes hacia los tejidos del organismo, transportar los productos de desecho, transportar las hormonas de una parte del organismo . En general, mantener un entorno apropiado en todos los líquidos tisulares del organismo para lograr la supervivencia y funcionalidad de las células .
El corazón y los vasos sanguíneos están controlados, a su vez, de forma que proporcionan el gasto cardíaco y la presión arterial necesarios para garantizar el flujo sanguíneo necesario.
CARACTERÍSTICAS FÍSICAS DE LA CIRCULACIÓN
La circulación está divida en circulación sistémica y circulación pulmonar. Como la circulación sistémica aporta el flujo sanguíneo a todos los tejidos del organismo excepto los pulmones, también se conoce como circulación mayor o circulación periférica.
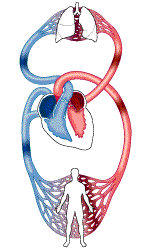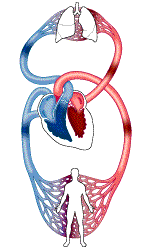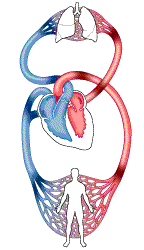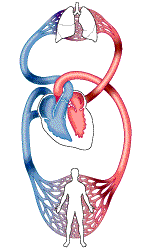
COMPONENTES FUNCIONALES DE LA CIRCULACIÓN
La función de las arterias consiste en transportar la sangre con una presión alta hacia los tejidos, motivo por el cual las arterias tienen unas paredes vasculares fuertes y unos flujos sanguíneos importantes con una velocidad alta.
Las arteriolas son las últimas ramas pequeñas del sistema arterial y actúan controlando los conductos a través de los cuales se libera la sangre en los capilares. Las arteriolas tienen paredes musculares fuertes que pueden cerrarlas por completo o que pueden, al relajarse, dilatar los vasos varias veces, con lo que pueden alterar mucho el flujo sanguíneo en cada lecho tisular en respuesta a sus necesidades.
La función de los capilares consiste en el intercambio de líquidos, nutrientes, electrólitos, hormonas y otras sustancias en la sangre y en el líquido intersticial. Para cumplir esta función, las paredes del capilar son muy finas y tienen muchos poros capilares diminutos, que son permeables al agua y a otras moléculas pequeñas.
Las vénulas recogen la sangre de los capilares y después se reúnen gradualmente formando venas de tamaño progresivamente mayor.
Las venas funcionan como conductos para el transporte de sangre que vuelve desde las vénulas al corazón; igualmente importante es que sirven como una reserva importante de sangre extra. Como la presión del sistema venoso es muy baja, las paredes de las venas son finas.
VOLÚMENES DE SANGRE EN LOS DISTINTOS COMPONENTES DE LA CIRCULACIÓN
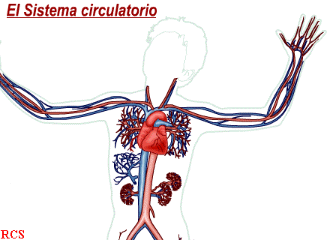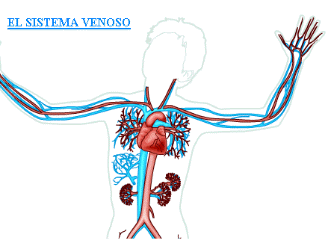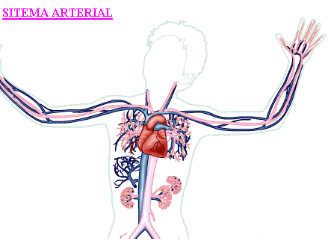
Aproximadamente el 84% de todo el volumen de sangre del organismo se encuentra en la circulación sistémica y el 16% en el corazón y los pulmones. Del 84% que está en la circulación sistémica, el 64% está en las venas, el 13% en las arterias y el 7% en las arteriolas y capilares sistémicos. El corazón contiene el 7% de la sangre y los vasos pulmonares, el 9%. Resulta sorprendente el bajo volumen de sangre que hay en los capilares, aunque es allí donde se produce la función más importante de la circulación, la difusión de las sustancias que entran y salen entre la sangre y los tejidos.
SUPERFICIES TRANSVERSALES Y VELOCIDADES DEL FLUJO SANGUINEO
Si todos los vasos sistémicos de cada tipo se pusieran uno al lado del otro, la superficie transversal total aproximada para un ser humano medio sería la siguiente .La superficie transversal es mucho mayor de las venas que de las arterias, con una media cuatro veces mayor en las primeras, lo que explica la gran capacidad de reserva de sangre en el sistema venoso comparado con el sistema arterial. Como debe pasar el mismo volumen de flujo sanguíneo (F) a través de cada segmento de la circulación en cada minuto, la velocidad del flujo sanguíneo (v) es inversamente proporcional a la superficie transversal vascular (A). v = F/A Es decir, en condiciones de reposo la velocidad es como media de 33 cm/s en la aorta pero con una velocidad sólo de 1/1.000 en los capilares, es decir, aproximadamente 0,3 mm/s. No obstante, como los capilares tienen una longitud de sólo 0,3 a 1 mm, la sangre sólo se queda allí durante 13 s.
DISTRIBUCION DEL VOLUMEN SANGUINEO POR PORCENTAJE
PRESIONES EN LAS DISTINTAS PORCIONES DE LA CIRCULACIÓN
El corazón bombea la sangre hacia la aorta, la presión media en este vaso es alta, con una media en torno a los 100 mmHg.El bombeo cardíaco es pulsátil, la presión arterial alterna entre una presión sistólica de 120 mmHg y una diastólica de 80 mmHg. A medida que el flujo sanguíneo atraviesa la circulación sistémica la presión media va cayendo progresivamente hasta llegar casi a 0 mmHg en el momento en el que alcanza la terminación de las venas cava, donde se vacía en la aurícula derecha del corazón. La presión de los capilares sistémicos oscila desde 35 mmHg cerca de los extremos arteriolares hasta tan sólo 10 mmHg cerca de los extremos venosos, pero la presión media «funcional» en la mayoría de los lechos vasculares es de 17 mmHg, una presión suficientemente baja que permite pequeñas fugas de plasma a través de los poros diminutos de las paredes capilares, aunque los nutrientes pueden difundir fácilmente a través de los mismos poros hacia las células de los tejidos externos.
PRINCIPIOS BASICOS DE LA FUNCIÓN CIRCULATORIA
La velocidad del flujo sanguíneo en cada tejido del organismo casi siempre se controla con precisión en relación con la necesidad del tejido.
El gasto cardíaco se controla principalmente por la suma de todos los flujos tisulares locales.
La regulación de la presión arterial es generalmente independiente del control del flujo sanguíneo local o del control del gasto cardíaco.
papel importante en el control de la presión, tanto al se gregar hormonas que controlan la presión como al regular el volumen de sangre.
INTERRELACIONES ENTRE LA PRESIÓN,FLUJO Y RESISTENCIA
El flujo sanguíneo que atraviesa un vaso sanguíneo está determinado por dos factores: 1) diferencia de presión de la sangre entre los dos extremos de un vaso, también denominado «gradiente de presión» en el vaso, que es la fuerza que empuja la sangre a través del vaso, y 2) los impedimentos que el flujo sanguíneo encuentra en el vaso, que se conoce como resistencia vascular.
Resultado de imagen para interrelacion entre presion flujo y resistencia
P1 representa la presión en el origen del vaso; en el otro extremo, la presión es P2. La resistencia es consecuencia de la fricción entre el flujo de sangre y el endotelio intravascular en todo el interior del vaso.
El flujo a través del vaso se puede calcular con la fórmula siguiente, que se conoce como ley de Ohm: F = ∆P/R en donde F es el flujo sanguíneo, ∆P es la diferencia de presión (P1 – P2) entre los dos extremos del vaso y R es la resistencia. En esta fórmula se afirma que el flujo sanguíneo es directamente proporcional a la diferencia de presión, pero inversamente proporcional a la resistencia.
FLUJO SANGUINEO
El flujo sanguíneo es la cantidad de sangre que atraviesa un punto dado de la circulación en un período de tiempo determinado. Se expresa en mililitros por minuto o litros por minuto, pero puede expresarse en mililitros por segundo o en cualquier otra unidad del flujo y de tiempo. El flujo sanguíneo global de toda la circulación de un adulto en reposo es de unos 5.000 ml/min, cantidad que se considera igual al gasto cardíaco porque es la cantidad de sangre que bombea el corazón en la aorta en cada minuto
MÉTODOS DE MEDICIÓN DEL FLUJO SANGUÍNEO
Se pueden introducir en serie muchos dispositivos mecánicos y electromecánicos dentro de un vaso sanguíneo o bien aplicarse en el exterior de la pared del vaso para medir el flujo. Este tipo de equipo se denomina flujómetro.
FLUJOMETRO ELECTROMAGNÉTICO
Uno de los dispositivos más importantes que permiten medir el flujo sanguíneo sin abrir el vaso es el flujómetro electromagnético, se muestra la generación de la fuerza electromotriz (voltaje eléctrico) de un cable que se mueve rápidamente atravesando un campo magnético. Este es el principio de producción de electricidad en un generador eléctrico,el mismo principio se aplica a la generación de una fuerza electromotriz en sangre que se está desplazando a través de un campo magnético. En este caso, se coloca un vaso sanguíneo entre los polos de un potente imán y se colocan los electrodos a ambos lados del vaso, perpendiculares a las líneas de fuerza magnéticas. Cuando el flujo sanguíneo atraviesa el vaso se genera entre los electrodos un voltaje eléctrico proporcional a la velocidad del flujo sanguíneo y el voltaje se registra usando un voltímetro o un aparato de registro electrónico apropiado. Una ventaja especial del flujómetro electromagnético es que puede registrar cambios del flujo en menos de 1/100 de segundo, con lo que se obtiene un registro exacto de los cambios pulsátiles del flujo y también de los valores en equilibrio.
FLUJÓMETRO ULTRASÓNICO DOPPLER
Se monta un cristal piezoeléctrico diminuto en el extremo de la pared del dispositivo. Cuando este cristal recibe la energía de un aparato eléctrico apropiado transmite una frecuencia de varios cientos de miles de ciclos por segundo distalmente sobre la sangre circulante. Una parte del sonido es reflejada por los eritrocitos de la sangre circulante y estas ondas de ultrasonidos reflejadas vuelven desde las células sanguíneas hacia el cristal con una frecuencia menor que la onda transmitida, porque los eritrocitos se están alejando del cristal transmisor. Es lo que se conoce como efecto Doppler , la onda de ultrasonido de alta frecuencia se interrumpe de forma intermitente y la onda reflejada vuelve hacia el cristal y se amplifica en el aparato electrónico, mientras que otra porción del mismo determina la diferencia de frecuencia entre la onda transmitida y la onda reflejada y, con ello, la velocidad del flujo sanguíneo. Siempre que no cambie el diámetro de un vaso sanguíneo, los cambios en el flujo sanguíneo en el vaso están relacionados directamente con las variaciones en la velocidad de flujo. El flujómetro ultrasónico Doppler puede registrar cambios pulsátiles .
FLUJO DE SANGRE LAMINAR EN LOS VASOS
Cuando el flujo sanguíneo se mantiene en equilibrio a través de un vaso sanguíneo largo y liso, el flujo se produce de forma aerodinámica, manteniéndose cada capa de sangre a la misma distancia de la pared del vaso. Además, la porción de sangre más central se mantiene en el centro del vaso. Este tipo de flujo se conoce como flujo laminar o flujo aerodinámico y es el contrario del flujo turbulento, que es el flujo sanguíneo que transcurre en todas las direcciones del vaso y se mezcla continuamente en su interior.
PERFIL DE VELOCIDAD PARABÓLICA DURANTE EL FLUJO LAMINAR
Cuando se produce el flujo laminar la velocidad del flujo en el centro del vaso es bastante mayor que la velocidad cerca de los bordes exteriores se muestra un vaso que contiene dos líquidos, el de la izquierda teñido con un colorante y el de la derecha, transparente, pero no hay flujo en el vaso. Cuando se hacen fluir, se desarrolla una interfase parabólica entre ellos, la porción de líquido adyacente a la pared del vaso apenas se ha movido, la que está algo alejada se ha desplazado una distancia pequeña y la que está en la porción central se ha desplazado mucho. Este efecto se conoce como el «perfil parabólico de la velocidad del flujo sanguíneo».
Resultado de imagen para velocidad parabolica durante el flujo laminar
La causa de este perfil parabólico es la siguiente: las moléculas de líquido que tocan la pared se mueven lentamen te por su adherencia a la pared del vaso. La siguiente capa de moléculas se desliza sobre ellas, la tercera capa sobre la segunda, la cuarta sobre la tercera, etc. Por tanto, el líquido de la parte central del vaso se puede mover rápidamente porque hay muchas capas de moléculas deslizantes entre la zona central del vaso y su pared.
FLUJO DE SANGRE TURBULENTO EN ALGUNAS SITUACIONES
Cuando la velocidad del flujo sanguíneo es demasiado grande, cuando atraviesa una obstrucción en un vaso, hace un giro brusco o pasa sobre una superficie rugosa, el flujo puede volverse turbulento o desordenado en lugar de aerodinámico. El flujo turbulento significa que el flujo sanguíneo atraviesa el vaso en dirección transversal y también longitudinal, formando espirales que se denominan corrientes en torbellino, Cuando hay corrientes en torbellino el flujo sanguíneo encuentra una resistencia mucho mayor que cuando el flujo es aerodinámico, porque los torbellinos aumentan mucho la fricción global del flujo en el vaso. El flujo turbulento tiende a aumentar en proporción directa a la velocidad del flujo sanguíneo, al diámetro del vaso sanguíneo y a la densidad de la sangre y es inversamente proporcional a la viscosidad de la sangre.
Re = ν.d.ρ/n
Re es el número de Reynolds, una medida que da idea de la tendencia a producirse turbulencias, ( es la velocidad media del flujo sanguíneo (en centímetros/segundo), d es el diámetro del vaso (en centímetros), ρ es la densidad y n es la viscosidad (en poise). La viscosidad de la sangre suele ser de 1/30 poise y la densidad es sólo ligeramente mayor de 1, por lo que un aumento del número de Reynolds por encima de 200400 indica que se producirá flujo turbulento en algunas ramas de los vasos.
Resultado de imagen para viscosidad de la sangre
condiciones apropiadas para que haya turbulencias: 1) una velocidad elevada del flujo sanguíneo 2) la naturaleza pulsátil del mismo; 3) el cambio brusco del diámetro del vaso, y 4) un diámetro del vaso de gran calibre.
PRESIÓN SANGUÍNEA
UNIDADES ESTÁNDAR DE PRESIÓN
La presión sanguínea se mide casi siempre en milímetros de mercurio (mmHg) porque el manómetro de mercurio se ha usado como patrón de referencia para medir la presión desde su invención en 1846 por Poiseuille. En realidad, la presión arterial mide la fuerza ejercida por la sangre contra una unidad de superficie de la pared del vaso.
Una presión de 1 mm de mercurio es igual a una presión de 1,36 cm de agua, porque la densidad del mercurio es 13,6 veces mayor que la del agua y 1 cm es 10 veces mayor que 1 mm.
RESISTENCIA AL FLUJO SANGUÍNEO
Unidades de resistencia. La resistencia es el impedimento al flujo sanguíneo en un vaso, pero no se puede medir por medios directos. Por el contrario, la resistencia debe calcularse a partir de las determinaciones del flujo sanguíneo y de la diferencia de presión entre dos puntos del vaso. Si la diferencia de presión entre los dos puntos es de 1 mmHg y el flujo es de 1 ml/s, se dice que la resistencia es de una unidad de resistencia periférica, abreviada habitualmente como PRU.
EXPRESIÓN DE LA RESISTENCIA EN UNIDADES CGS
En ocasiones se usa una unidad física básica en CGS (centímetros, gramos, segundos) para expresar la resistencia. Esta unidad es la dina · s/cm5. La resistencia en esas unidades puede calcularse mediante la fórmula siguiente: R(en dina . s /cm5 ) = 1.333 × mmHg /ml/s
RESISTENCIA VASCULAR PERIFÉRICA TOTAL Y RESISTENCIA VASCULAR PULMONAR TOTAL
La velocidad del flujo sanguíneo a través de todo el sistema circulatorio es igual a la velocidad de la sangre que bombea el corazón. En un ser humano adulto es aproximadamente igual a 100 ml/s. La diferencia de presión entre las arterias sistémicas y las venas sistémicas es de unos 100 mmHg. Por tanto, la resistencia de toda la circulación sistémica, que se denomina resistencia periférica total, es de 100/100no 1 unidad de resistencia periférica PRU.
Resultado de imagen para sistema vascular del corazon y pulmonar
En el sistema pulmonar la presión arterial media es de 16 mmHg y la presión media en la aurícula izquierda es de 2 mmHg, con lo que la diferencia neta de presión es de 14 mm. Cuando el gasto cardíaco es normal, en torno a 100 ml/s, se calcula que la resistencia vascular pulmonar total es de 0,14 PRU (la séptima parte que en la circulación sistémica)
CONDUCTANCIA DE LA SANGRE EN UN VASO Y SU RELACIÓN CON LA RESISTENCIA
La conductancia es la medición del flujo sanguíneo a través de un vaso para dar una diferencia de presión dada. Se expresa en milímetros por segundo por milímetro de mercurio de presión, pero también se puede expresar en litros por segundo por milímetro de mercurio o en cualquier otra unidad del flujo sanguíneo y presión. Es evidente que la conductancia es el recíproco exacto de la resistencia según la ecuación: Conductancia = 1 /Resistencia
CAMBIOS MUY PEQUEÑOS EN EL DIÁMETRO DE UN VASO CAMBIAN MUCHO LA CONDUCTANCIA
Pequeños cambios en el diámetro de un vaso provocan cambios enormes en su capacidad de conducir la sangre cuando el flujo sanguíneo es aerodinámico.
LEY DE POISEUILLE
la sangre que está cerca de la pared de los vasos fluye lentamente, mientras que la que está en el centro del vaso fluye mucho más rápidamente. En el vaso pequeño, esencialmente toda la sangre está cerca de la pared, por lo que, sencillamente, no existe un chorro central de sangre que fluya con gran rapidez. Al integrar las velocidades de todos los anillos concéntricos de la sangre en movimiento y multiplicarlos por las superficies de los anillos se puede obtener la fórmula siguiente, que representa la ley de Poiseuille: F = π∆ Pr4 _ 81 en la que F es la velocidad del flujo sanguíneo, ∆P es la diferencia de presión entre los extremos del vaso, r es el radio del vaso, l es la longitud del vaso y es la viscosidad de la sangre.En esta ecuación la velocidad del flujo sanguíneo es directamente proporcional a la cuarta potencia del radio del vaso, por lo tanto diámetro de un vaso sanguíneo es el que tiene la mayor importancia entre todos estos factores para determinar la velocidad del flujo sanguíneo a través del vaso.
IMPORTANCIA DE LA LEY DE LA CUARTA POTENCIA DEL DIÁMETRO DEL VASO PARA DETERMINAR LA RESISTENCIA ARTERIOLAR
En la circulación sistémica, aproximadamente dos tercios de toda la resistencia sistémica al flujo sanguíneo se debe a la resistencia arteriolar en las pequeñas arteriolas. Los diámetros internos de las arteriolas varían desde tan sólo 4 mm hasta 25 mm, la ley de la cuarta potencia relaciona el vaso sanguíneo con el diámetro del vaso, se puede ver que este incremento en cuatro veces del diámetro del vaso aumenta el flujo hasta en 256 veces, es decir, esta ley de cuarta potencia hace que sea posible que las arteriolas, que responden con sólo pequeños cambios del diámetro a las señales nerviosas o a las señales químicas de los tejidos locales, hagan desaparecer casi completamente el flujo sanguíneo hacia el tejido o vayan al otro extremo, provocando un inmenso incremento del flujo.
RESISTENCIA AL FLUJO SANGUÍNEO EN CIRCUITO VASCULARES EN SERIE Y PARALELO
La sangre que bombea el corazón fluye desde la parte de presión alta de la circulación sistémica (es decir, la aorta) hacia el lado de baja presión a través de muchos miles de vasos sanguíneos dispuestos en serie y en paralelo. Las arterias, arteriolas, capilares, vénulas y venas se disponen colectivamente en serie. Cuando esto sucede, el flujo de cada vaso sanguíneo es el mismo y la resistencia total al flujo sanguíneo (Rtotal) es igual a la suma de la resistencia de cada vaso:
R total = R1 + R2 + R3 + R4
La resistencia vascular periférica total es igual a la suma de resistencias de las arterias, arteriolas, capilares, vénulas y venas.
En el ejemplo que se ve en la figura 149A, la resistencia vascular total es igual a la suma de R1 y R2. Los vasos sanguíneos emiten numerosas ramas que forman circuitos paralelos que aportan la sangre a los distintos órganos y tejidos del organismo. Esta distribución paralela permite que cada tejido regule su propio flujo sanguíneo en mayor grado, independientemente del flujo de los demás tejidos. En cuanto a los vasos sanguíneos en paralelo ( fig. 149B), la resistencia total al flujo sanguíneo se expresa como: 1 _ Rtotal = 1 _ R1 + 1 _ R2 + 1 _ R3 + 1 _ R4 … Es evidente que, para un gradiente de resistencia dado, fluirán cantidades de sangre mucho mayores a través de este sistema paralelo que a través de cada uno de los vasos sanguíneos por separado, por lo que la resistencia total es bastante menor que la resistencia de cualquier vaso sanguíneo aislado. El flujo a través de cada uno de los vasos unidos en paralelo de la figura 149B está determinado por el gradiente de presión y su propia resistencia, y no la resistencia de los demás vasos sanguíneos en paralelo. No obstante, el aumento de la resistencia de cualquiera de los vasos sanguíneos aumenta la resistencia vascular total. Si hay muchos vasos sanguíneos en paralelo será más sencillo para la sangre fluir a través del circuito porque cada vaso paralelo constituye otra vía o conductancia para el flujo sanguíneo.
La conductancia total (Ctotal) del flujo sanguíneo es la suma de la conductancia de cada vía paralela: C total = C1 + C2 + C3 + C4
EFECTO DEL HEMATOCRITO Y DE LA VISCOSIDAD DE LA SANGRE SOBRE LA RESISTENCIA VASCULAR Y EL FLUJO SANGUÍNEO
Otro de los factores importantes de la ley de Poiseuille es la viscosidad de la sangre. Cuanto mayor sea la viscosidad, menor será el flujo en un vaso si todos los demás factores se mantienen constantes. Además, la viscosidad de la sangre normal es tres veces mayor que la viscosidad del agua. Pero ¿qué hace que la sangre sea tan viscosa? Principalmente, el gran número de hematíes suspendidos en la sangre.
HEMATOCRITO
La proporción de la sangre que corresponde a glóbulos rojos se conoce como hematocrito, es decir, si una persona tiene un hematocrito de 40 significa que el 40% del volumen sanguíneo está formado por las células y el resto es plasma. El hematocrito de un varón adulto alcanza un promedio de 42, mientras que en las mujeres es de 38.
El hematocrito se determina centrifugando la sangre en el tubo calibrado.
EFECTO DEL HEMATOCRITO SOBRE LA VISCOSIDAD DE LA SANGRE
La viscosidad de la sangre aumenta drásticamente a medida que lo hace el hematocrito. La viscosidad de la sangre total con un hematocrito normal es de 3, lo que significa que se necesita tres veces más presión para obligar a la sangre total a atravesar un vaso que si fuera agua. Cuando el hematocrito aumenta hasta 60 o 70, como sucede en caso de policitemia, la viscosidad de la sangre puede ser hasta 10 veces mayor que la del agua y su flujo a través de los vasos sanguíneos se retrasa mucho. Otros factores que afectan a la viscosidad de la sangre son la concentración y el tipo de las proteínas plasmáticas. La viscosidad del plasma sanguíneo es 1,5 veces la del agua.
EFECTOS DE LA PRESIÓN SOBRE LA RESISTENCIA VASCULAR Y EL FLUJO SANGUÍNEO TISULAR
La «autorregulación» atenúa el efecto de la presión arterial en el flujo sanguíneo tisular. El incremento de la presión arterial debería provocar un incremento proporcional del flujo sanguíneo en los distintos tejidos del organismo. La razón de este incremento es que el aumento de la presión arterial no sólo aumenta la fuerza que impulsa la sangre a través de los vasos, sino que también inicia incrementos compensatorios en la resistencia vascular a través de la activación de los mecanismos locales de control. De modo inverso, con las reducciones en la presión arterial, la mayor parte de la resistencia vascular se reduce en un tiempo breve en los tejidos y el flujo sanguíneo se mantiene relativamente constante. La capacidad de cada tejido de ajustar su resistencia vascular y mantener un flujo sanguíneo normal durante los cambios en la presión arterial entre aproximadamente 70 y 175 mmHg se denomina AUTORREGULACIÓN DEL FLUJO SANGUÍNEO.
Los cambios del flujo sanguíneo se pueden provocar mediante la estimulación simpática, que constriñe los vasos sanguíneos periféricos. Análogamente, los vasoconstrictores hormonales, como noradrenalina, angiotensina II, vasopresina o endotelina, también pueden reducir el flujo sanguíneo.
RELACIÓN PRESIÓN-FLUJO EN LOS LECHOS VASCULARES PASIVOS
En vasos sanguíneos aislados o en tejidos que no muestran autorregulación, los cambios en la presión arterial pueden tener efectos importantes en el flujo sanguíneo. El motivo es que el aumento de la presión arterial no sólo incrementa la fuerza que impulsa la sangre a través de los vasos sino que además distiende los vasos elásticos, para reducir en la práctica la resistencia vascular. Inversamente, el descenso en la presión arterial en vasos sanguíneos pasivos eleva la resistencia, ya que los vasos elásticos se colapsan gradualmente debido a la reducción en la presión de distensión. Cuando la presión desciende por debajo de un nivel crítico, denominado presión de cierre crítica, el flujo cesa en el momento en que los vasos sanguíneos se colapsan por completo. La estimulación simpática y otros vasoconstrictores pueden alterar la relación de flujopresión.
Imagen relacionada
la inhibición de la actividad simpática dilata mucho los vasos y aumenta el flujo sanguíneo al doble o más. Por el contrario, una estimulación simpática potente contrae los vasos tanto que, en ocasiones, el flujo sanguíneo disminuye casi a cero durante unos segundos
Bradon nazario vazquez balanzar
EXCITACIÓN RITMICA DEL CORAZÓN
El corazón está dotado de un sistema especial para generar impulsos eléctricos rítmicos para producir la contracción rítmica del músculo cardíaco y tambien conducir estos estímulos rápidamente por todo el corazón.
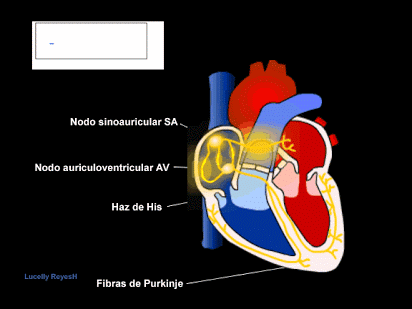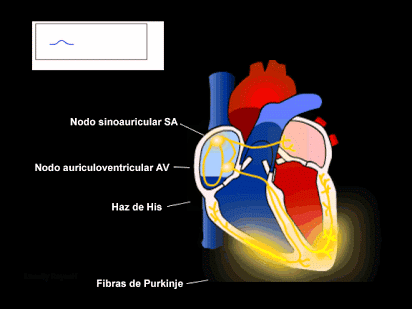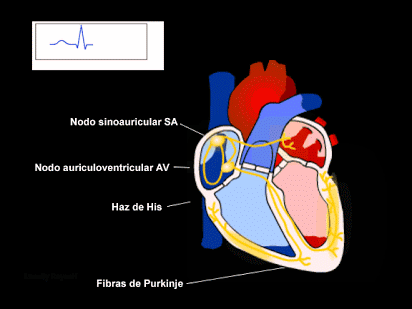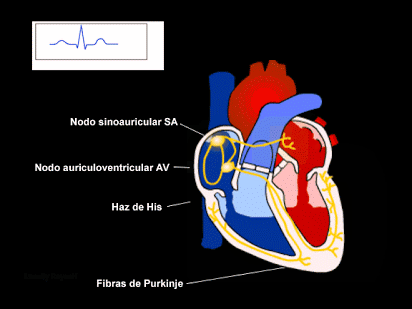
Cuando este sistema funciona normalmente, las aurículas se contraen aproximadamente 1/6 de segundo antes de la contracción ventricular, lo que permite el llenado de los ventrículos antes de que bombeen la sangre a través de los pulmones y de la circulación periférica.
Este sistema rítmico y de conducción del corazón se puede lesionar en las cardiopatías, especialmente en la isquemia de los tejidos cardíacos que se debe a una disminución del flujo sanguíneo coronario. La consecuencia es con frecuencia una alteración del ritmo cardíaco o una secuencia anormal de contracción de las cavidades cardíacas.
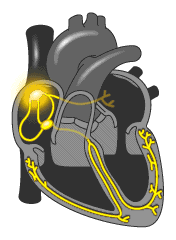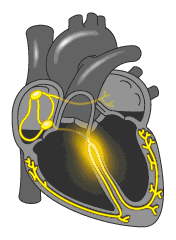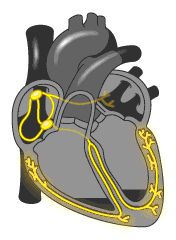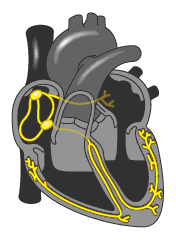
SISTEMA DE EXCITACIÓN ESPECIALIZADO Y DE CONDUCCIÓN DEL CORAZÓN
En este sistema tendremos e nódulo sinusal (también denominado nódulo sinoauricular o SA), en el que se genera el impulso rítmico normal; las vías internodulares que conducen impulsos desde el nódulo sinusal hasta el nódulo auriculoventricular (AV); el nódulo AV, en el cual los impulsos originados en las aurículas se retrasan antes de penetrar en los ventrículos; el haz AV, que conduce impulsos desde las aurículas hacia los ventrículos, y las ramas izquierda y derecha del haz de fibras de Purkinje, que conducen los impulsos cardíacos por todo el tejido de los ventrículos.
NÓDULO SINUSAL(SINOAURICULAR)
El nódulo sinusal (también denominado nódulo sinoauricular) es una banda elipsoide, aplanada y pequeña de músculo cardíaco especializado de aproximadamente 3 mm de anchura, 15 mm de longitud y 1 mm de grosor. Está localizado en la pared posterolateral superior de la aurícula derecha, inmediatamente inferior y ligeramente lateral a la desembocadura de la vena cava superior.
Las fibras del nódulo sinusal se conectan directamente con las fibras musculares auriculares, de modo que todos los potenciales de acción que comienzan en el nódulo sinusal se propagan inmediatamente hacia la pared del músculo auricular.
RITMICIDAD ELÉCTRICA AUTOMÁTICA DE LAS FIBRAS SINUSALES
Algunas fibras cardíacas tiene la capacidad de autoexcitación, que es un proceso que puede producir descargas y contracciones rítmicas automáticas. Esto es especialmente cierto en el caso de las fibras del sistema especializado de conducción del corazón, entre ellas las fibras del nódulo sinusal. Por este motivo el nódulo sinusal habitualmente controla la frecuencia del latido de todo el corazón.
MECANISMOS DE LA RITMICIDAD DEL NÓDULO SINUSAL
Muestra potenciales de acción registrados desde el interior de una fibra del nódulo sinusal durante tres latidos cardíacos y, a modo de comparación, un único potencial de acción de una fibra muscular ventricular.Entre descargas el «potencial de membrana en reposo» de la fibra del nódulo sinusal tiene una negatividad de aproximadamente –55 a –60 mV, en comparación con –85 a –90 mV para la fibra muscular ventricular. La causa de esta menor negatividad es que las membranas celulares de las fibras sinusales son permeables naturalmente a los iones sodio y calcio, y las cargas positivas de los iones sodio y calcio que entran neutralizan parte de la negatividad intracelular.
El músculo cardíaco tiene tres tipos de canales iónicos de membrana que tienen funciones importantes en la generación de los cambios de voltaje en el potencial de acción. Los tipos son:
1) los canales rápidos de sodio
2) los canales lentos de sodio-calcio
3) los canales de potasio.
La apertura de los canales rápidos de sodio es responsable de la rápida espiga ascendente del potencial de acción que se observa en el músculo ventricular, debido a la entrada rápida de iones sodio positivos hacia el interior de la fibra. Después, la «meseta» del potencial de acción ventricular está producida por la apertura lenta de los canales lentos de sodiocalcio, que dura aproximadamente 0,3 s. Finalmente, la apertura de los canales de potasio permite la difusión de grandes cantidades de iones potasio positivos hacia el exterior a través de la membrana de la fibra y devuelve el potencial de membrana a su nivel de reposo.
Hay una diferencia en la función de estos canales en la fibra del nódulo sinusal porque el potencial «de reposo» es mucho menos negativo (de sólo –55 mV en la fibra nodular, en lugar de los –90 mV de la fibra muscular ventricular). A este nivel de –55 mV, los canales rápidos de sodio principalmente ya se han «inactivado», lo que significa que han sido bloqueados. La causa de esto es que siempre que el potencial de membrana es menos negativo –55 mV durante más de algunos milisegundos, las compuertas inactivación del interior de la membrana celular que cierran los canales rápidos de sodio se cierran y permanecen de esta manera.
Por tanto, sólo se pueden abrir los canales lentos de sodiocalcio (es decir, se pueden «activar») y, por tanto, pueden producir el potencial de acción. En consecuencia, el potencial de acción del nódulo auricular se produce más lentamente que el potencial de acción del músculo ventricular.
AUTOEXCITACIÓN DE LAS FIBRAS DEL NÓDULO SINUSAL
Debido a la elevada concentración de iones sodio en el líquido extracelular en el exterior de la fibra nodular, así como al número moderado de canales de sodio abiertos previamente, los iones sodio positivos del exterior de las fibras normalmente tienden a desplazarse hacia el interior. Por tanto, entre los latidos cardíacos, la entrada de iones sodio de carga positiva produce una elevación lenta del potencial de membrana en
reposo en dirección positiva. El potencial «en reposo» aumenta gradualmente y se hace menos negativo entre cada dos latidos sucesivos. Cuando el potencial alcanza un voltaje umbral de aproximadamente –40 mV, los canales de sodiocalcio se «activan», produciendo de esta manera el potencial de acción.
LA PERMEABILIDAD INHERENTE DE LAS FIBRAS DEL NÓDULO SINUSAL A LOS IONES SODIO Y CALCIO PRODUCE SU AUTOEXCITACIÓN.
¿Por qué esta permeabilidad a los iones sodio y calcio no hace que las fibras del nódulo sinusal permanezcan despolarizadas todo el tiempo? La respuesta es que durante el transcurso del potencial de acción se producen dos fenómenos que lo impiden. Primero, los canales de sodiocalcio se inactivan en un plazo de aproximadamente 100 a 150 ms después de su apertura, y segundo, aproximadamente al mismo tiempo se abren números muy elevados de canales de potasio. Por tanto, se interrumpe el flujo de entrada de iones positivos calcio y sodio a través de los canales de sodiocalcio, mientras que al mismo tiempo grandes cantidades de iones positivos de potasio difunden hacia el exterior de la fibra. Estos dos efectos reducen el potencial intracelular hasta devolverlo a su nivel de reposo negativo y, por tanto, ponen fin al potencial de acción.
El estado de hiperpolarización inicialmente desplaza el potencial de membrana «en reposo» hacia abajo hasta aproximadamente –55 o –60 mV al final del potencial de acción. ¿Por qué este nuevo estado de hiperpolarización no se mantiene indefinidamente? El motivo es que en las décimas de segundo siguientes al final del potencial de acción se cierran cada vez más canales de potasio. Los iones sodio y calcio que fluyen hacia el interior una vez más compensan el flujo de salida de iones potasio, y esto hace que el potencial «de reposo» se desplace hacia arriba una vez más, alcanzando finalmente el nivel liminal de aproximadamente –40 mV. Después comienza de nuevo todo el proceso: autoexcitación .
VÍAS INTERNODULARES Y TRANSMISIÓN DEL IMPULSO CARDÍACO A TRAVÉS DE LAS AURÍCULAS
Los extremos de las fibras del nódulo sinusal se conectan directamente con las fibras musculares auriculares circundantes. Por tanto, los potenciales de acción que se originan en el nódulo sinusal viajan hacia estas fibras musculares auriculares. De esta manera, el potencial de acción se propaga por toda la masa muscular auricular y, finalmente, llega hasta el nódulo AV.
La velocidad de conducción en la mayor parte del músculo auricular es de aproximadamente 0,3 m/s, pero la conducción es más rápida, de aproximadamente 1 m/s, en varias pequeñas bandas de fibras auriculares. Una de ellas, denominada banda interauricular anterior, atraviesa las paredes anteriores de las aurículas para dirigirse hacia la aurícula izquierda. Además, otras tres bandas pequeñas se incurvan a través de las paredes auriculares anterior, lateral y posterior, y terminan en el nódulo AV; se denominan, vías internodulares anterior, media y posterior. La causa de la velocidad de conducción más rápida de estas bandas es la presencia de fibras de conducción especializadas.
NÓDULO AURICULOVENTRICULAR Y RETRASO DE LA CONDUCCIÓN DEL IMPULSO DESDE LAS AURICULAS A LOS VENTRICULOS
El sistema de conducción auricular está organizado de modo que el impulso cardíaco no viaja desde las aurículas hacia los ventrículos demasiado rápidamente; este retraso da tiempo para que las aurículas vacíen su sangre hacia los ventrículos antes de que comience la contracción ventricular.
El retraso de la transmisión hacia los ventrículos se produce principalmente en el nódulo AV y en sus fibras de conducción adyacentes. El nódulo AV está localizado en la pared posterolateral de la aurícula derecha, inmediatamente detrás de la válvula tricúspide.
Obsérvese que el impulso, después de viajar por las vías internodulares, llega al nódulo AV aproximadamente 0,03 s después de su origen en el nódulo sinusal. Después hay un retraso de otros 0,09 s en el propio nódulo AV antes de que el impulso entre en la porción penetrante del haz AV, a través del cual pasa hacia los ventrículos. Se produce un retraso final de otros 0,04 s principalmente en este haz AV penetrante, que está formado por múltiples fascículos pequeños que atraviesan el tejido fibroso que separa las aurículas de los ventrículos.
Así, el retraso total en el nódulo AV y en el sistema de AV es de aproximadamente 0,13 s. Esto, añadido al retraso inicial de la conducción de 0,03 s desde el nódulo sinusal hasta el nódulo AV, hace que haya un retraso total de 0,16 s antes de que la señal excitadora llegue finalmente al músculo ventricular que se está contrayendo.
CAUSA DE LA CONDUCCIÓN LENTA
La conducción lenta en las fibras transicionales, nodulares y penetrantes del haz AV está producida principalmente por la disminución del número de uniones en hendidura entre células sucesivas de las vías de conducción, de modo que hay una gran resistencia a la conducción de los iones excitadores desde una fibra de conducción hasta la siguiente. Por tanto, es fácil ver por qué se tarda en excitar células sucesivas.
TRANSMISIÓN RÁPIDA EN EL SISTEMA DE PURKINJE VENTRICULAR
Las fibras de Purkinje especiales se dirigen desde el nódulo AV a través del haz AV hacia los ventrículos. Excepto en la porción inicial de estas fibras, donde penetran en la barrera fibrosa AV, tienen características funcionales bastante distintas a las de las fibras del nódulo AV. Son fibras muy grandes, incluso mayores que las fibras musculares ventriculares normales, y transmiten potenciales de acción a una velocidad de 1,5 a 4,0 m/s, una velocidad aproximadamente 6 veces mayor que la del músculo ventricular normal y 150 veces mayor que la de algunas de las fibras del nódulo AV. Esto permite una transmisión casi instantánea del impulso cardíaco por todo el resto del músculo ventricular.
CONDUCCIÓN UNIDIRECCIONAL A TRAVÉS DEL HAZ AV
Una característica especial del haz AV es la imposibilidad, excepto en estados anormales, de que los potenciales de acción viajen retrógradamente desde los ventrículos hacia las aurículas. Esto impide la reentrada de los impulsos cardíacos por esta ruta desde los ventrículos hacia las aurículas, permitiendo sólo la contracción anterógrada desde las aurículas hacia los ventrículos. Además, se debe recordar que en todas las localizaciones excepto en el haz AV el músculo auricular está separado del músculo ventricular por una barrera fibrosa continua. Esta barrera normalmente actúa como aislante para impedir el paso de los impulsos cardíacos entre el músculo auricular y ventricular a través de cualquier ruta distinta a la conducción anterógrada a través del propio haz AV.
DISTRIBUCIÓN DE LAS FIBRAS DE PURKINJE EN LOS VENTRICULOS:LAS RAMAS IZQUIERDA Y DERECHA DEL HAZ
Después de penetrar en el tejido fibroso que está entre el músculo auricular y ventricular, la porción distal del haz AV se dirigía hacia abajo en el interior del tabique interventricular a lo largo de 5 a 15 mm hacia la punta del corazón. Después el haz se divide en las ramas izquierda y derecha del haz, que están debajo del endocardio en los dos lados respectivos del tabique interventricular. Cada una de las ramas se dirige hacia abajo, hacia la punta del ventrículo, dividiéndose progresivamente en ramas más pequeñas. Estas ramas, a su vez, siguen un trayecto en dirección lateral alrededor de cada una de las cavidades ventriculares y hacia atrás, hacia la base del corazón. Los extremos de las fibras de Purkinje penetran en aproximadamente un tercio del grosor de la masa muscular y finalmente se continúan con las fibras musculares cardíacas.
Desde el momento en el que el impulso cardíaco entre las ramas del haz en el tabique interventricular hasta que sale de las terminaciones de las fibras de Purkinje el tiempo total transcurrido es en promedio de sólo 0,03 s. Por tanto, una vez que el impulso cardíaco ha entrado en el sistema de conducción ventricular de Purkinje, se propaga casi inmediatamente a toda la masa del músculo ventricular.
TRANSMISIÓN DEL IMPULSO CARDÍACO EN EL MÚSCULO VENTRICULAR
Una vez que el impulso llega a los extremos de las fibras de Purkinje se transmite a través de la masa del músculo ventricular por las propias fibras musculares ventriculares. La velocidad de transmisión es ahora sólo de 0,3 a 0,5 m/s, una sexta parte de la velocidad de las fibras de Purkinje. El músculo cardíaco envuelve el corazón en una doble espiral, con tabiques fibrosos entre las capas en espiral; por tanto, el impulso cardíaco no viaja necesariamente directamente hacia el exterior, hacia la superficie del corazón, sino que se angula hacia la Superficie a lo largo de las direcciones de las espirales. Debido a esto, la transmisión desde la superficie endocárdica a la superficie epicárdica del ventrículo precisa hasta otros 0,03 s.El tiempo total para la transmisión del impulso cardíaco desde las ramas iniciales del haz hasta las últimas fibras del músculo ventricular en el corazón normal es de aproximadamente 0,06 s.
RESUMEN DE LA PROPAGACIÓN DEL IMPULSO CARDÍACO A TRAVÉS DEL CORAZÓN
Los números de la figura representan los intervalos de tiempo, en fracciones de segundo, que transcurren desde el origen del impulso cardíaco en el nódulo sinusal hasta su aparición en cada uno de los puntos respectivos del corazón. Obsérvese que el impulso se propaga a una velocidad moderada a través de las aurículas, aunque se retrasa más de 0,1 s en la región del nódulo AV antes de aparecer en el haz AV del tabique interventricular. Una vez que ha entrado en este haz, se propaga muy rápidamente a través de las fibras de Purkinje por todas las superficies endocárdicas de los ventrículos. Después el impulso se propaga de nuevo algo más lentamente a través del músculo ventricular hacia las superficies epicárdicas.
CONTROL DE LA EXCITACIÓN Y LA CONDUCCIÓN EN EL CORAZÓN
NÓDULO SINUSAL COMO MARCAPASOS DEL CORAZÓN
El impulso normalmente se origina en el nódulo sinusal. En algunas situaciones anormales no ocurre así. Otras partes del corazón pueden presentar también una excitación rítmica intrínseca de la misma forma que lo hacen las fibras del nódulo sinusal; esto es particularmente cierto en el caso de las fibras del nódulo AV y de las fibras de Purkinje. Las fibras del nódulo AV, cuando no son estimuladas por alguna fuente externa, descargan a una frecuencia rítmica intrínseca de 40 a 60 veces por minuto, y las fibras de Purkinje lo hacen a una frecuencia de entre 15 y 40 veces por minuto. Estas frecuencias son distintas a la frecuencia normal del nódulo sinusal, de 70 a 80 veces por minuto.
¿Por qué entonces es el nódulo sinusal, y no el nódulo AV ni las fibras de Purkinje, el que controla la ritmicidad del corazón? La frecuencia de descarga del nódulo sinusal es mayor que la frecuencia de descarga autoexcitadora natural de las fibras del nódulo AV y de las fibras de Purkinje. Cada vez que se produce una descarga en el nódulo sinusal su impulso se conduce hacia el nódulo AV y hacia las fibras de Purkinje, produciendo también la descarga de sus membranas. Pero el nódulo sinusal produce una nueva descarga antes de que las fibras del nódulo AV o las fibras de Purkinje puedan alcanzar sus propios umbrales de autoexcitación. Por tanto, el nuevo impulso procedente del nódulo sinusal descarga tanto las fibras del nódulo AV como las fibras de Purkinje antes de que se pueda producir autoexcitación en cualquiera de esas estructuras. El el nódulo sinusal controla el latido del corazón porque su frecuencia de descarga rítmica es más rápida que la de cualquier otra parte del corazón.
IMPORTANCIA DEL SISTEMA DE PURKINJE EN LA GENERACIÓN DE LA CONTRACCIÓN SINCRÓNICA DEL MÚSCULO VENTRICULAR
Normalmente el impulso cardíaco llega a casi todas las porciones de los ventrículos en un breve intervalo de tiempo, excitando la primera fibra muscular ventricular sólo 0,03 a 0,06 s antes de la excitación de la última. Esto hace que todas las porciones del músculo de los dos ventrículos comiencen a contraerse casi al mismo tiempo y que después sigan contrayéndose durante aproximadamente otros 0,3 s. La función de bomba eficaz de las dos cavidades ventriculares precisa este tipo sincrónico de contracción. Si el impulso cardíaco viajara lentamente a través de los ventrículos, buena parte de la masa ventricular se contraería antes de la contracción del resto, en cuyo caso se produciría una gran disminución de la función global de bomba. De hecho, en algunos tipos de trastornos cardíacos,se produce una transmisión lenta, y la eficacia del bombeo de los ventrículos disminuye hasta el 20-30%.
CONTROL DEL RITMO CARDÍACO Y LA CONDUCCIÓN DE IMPULSOS POR LOS NERVIOS CARDÍACOS: LOS NERVIOS SIMPÁTICOS Y PARASIMPÁTICOS
El corazón está inervado por nervios simpáticos y parasimpáticos, Los nervios parasimpáticos (vagos) se distribuyen principalmente a los nódulos SA y AV, en mucho menor grado al músculo de las dos aurículas y apenas directamente al músculo ventricular. Por el contrario, los nervios simpáticos se distribuyen en todas las regiones del corazón, con una intensa representación en el músculo ventricular, así como en todas las demás zonas.
LA ESTIMULACIÓN PARASIMPÁTICA (VAGAL) PUEDE RETRASAR O BLOQUEAR EL RITMO Y LA CONDUCCIÓN CARDIACA( ESCAPE VENTRICULAR)
La estimulación de los nervios parasimpáticos que llegan al corazón (los vagos) hace que se libere la hormona acetilcolina en las terminaciones nerviosas. Esta hormona tiene dos efectos principales sobre el corazón. Primero, reduce la frecuencia del ritmo del nódulo sinusal, y segundo, reduce la excitabilidad de las fibras de la unión AV entre la musculatura auricular y el nódulo AV, retrasando de esta manera la transmisión del impulso cardíaco hacia los ventrículos.
Una estimulación vagal débil a moderada reduce la frecuencia del bombeo del corazón, con frecuencia hasta un valor tan bajo como la mitad de lo normal. La estimulación intensa de los nervios vagos puede interrumpir completamente la excitación rítmica del nódulo sinusal o puede bloquear completamente la transmisión del impulso cardíaco desde las aurículas hacia los ventrículos a través del nódulo AV. Los ventrículos dejan de latir durante 5 a 20 s, pero después algún área pequeña de las fibras de Purkinje, habitualmente en la porción del tabique interventricular del haz AV, presenta un ritmo propio y genera la contracción ventricular a una frecuencia de 15 a 40 latidos por minuto. Este fenómeno se denomina escape ventricular.
MECANISMOS DE LOS EFECTOS VAGALES
La acetilcolina que se libera en las terminaciones nerviosas vagales aumenta mucho la permeabilidad de las membranas de las fibras a los iones potasio, lo que permite la salida rápida de potasio desde las fibras del sistema de conducción. Esto da lugar a un aumento de la negatividad en el interior de las fibras, un efecto que se denomina hiperpolarización, que hace que este tejido excitable sea mucho menos excitable. En el nódulo sinusal, el estado de hiperpolarización reduce el potencial de membrana «en reposo» de las fibras del nódulo sinusal a un nivel mucho más negativo de lo habitual, hasta –65 a –75 mV en lugar del nivel normal de –55 a –60 mV.
Por tanto, el aumento inicial del potencial de membrana del nódulo sinusal que produce la corriente de entrada de sodio y de calcio tarda mucho más en alcanzar el potencial liminal para la excitación. Esto retrasa mucho la frecuencia de ritmicidad de estas fibras nodulares. Si la estimulación vagal es lo suficientemente intensa es posible detener totalmente la autoexcitación rítmica de este nódulo. En el nódulo AV, el estado de hiperpolarización producido por la estimulación vagal hace que sea difícil que las pequeñas fibras auriculares que entran en el nódulo generen una corriente de una intensidad suficiente como para excitar las fibras nodulares. Por tanto, el factor de seguridad para la transmisión del impulso cardíaco a través de las fibras de transición hacia las fibras del nódulo AV disminuye.
EFECTO DE LA ESTIMULACIÓN SIMPÁTICA SOBRE EL RITMO Y LA CONDUCCIÓN DEL CORAZÓN
La estimulación simpática produce esencialmente los efectos contrarios sobre el corazón a los que produce la estimulación vagal.Primero, aumenta la frecuencia de descarga del nódulo sinusal. Segundo, aumenta la velocidad de conducción, así como el nivel de excitabilidad de todas las porciones del corazón. Tercero, aumenta mucho la fuerza de contracción de toda la musculatura cardíaca, tanto auricular como ventricular.La estimulación simpática aumenta la actividad global del corazón. La estimulación máxima casi puede triplicar la frecuencia del latido cardíaco y puede aumentar la fuerza de la contracción del corazón hasta dos veces.
MECANISMO DEL EFECTO SIMPÁTICO
La estimulación de los nervios simpáticos libera la hormona noradrenalina en las terminaciones nerviosas simpáticas. La noradrenalina estimula, a su vez, los receptores b1-adrenérgicos, que median en los efectos sobre la frecuencia cardíaca, aumenta la permeabilidad de la membrana de las fibras a los iones sodio y calcio. En el nódulo sinusal, un aumento de la permeabilidad a sodio-calcio genera un potencial en reposo más positivo y también produce un aumento de la velocidad del ascenso del potencial de membrana diastólico hacia el nivel liminal para la autoexcitación, acelerando de esta forma la autoexcitación y, por tanto, aumentando la frecuencia cardíaca.
En el nódulo AV y en los haces AV, el aumento de la permeabilidad a sodiocalcio hace que sea más fácil que el potencial de acción excite todas las porciones sucesivas de los haces de las fibras de conducción, disminuyendo de esta manera el tiempo de conducción desde las aurículas hasta los ventrículos. El aumento de la permeabilidad a los iones calcio es responsable al menos en parte del aumento de la fuerza contráctil del músculo cardíaco bajo la influencia de la estimulación simpática, porque los iones calcio tienen una función importante en la excitación del proceso contráctil de las miofibrillas.
Brandon Nazario vazquez balanzar
UNIDAD 3: EL CORAZÓN
CAPÍTULO 9: MÚSCULO CARDÍACO
El corazón esta formado realmente por dos bombas separadas: un corazón derecho que bombea sangre hacia los pulmones y un corazón izquierdo que bombea sangre a través de la circulación sistémica que aporta flujo sanguíneo a los demás órganos y tejidos del cuerpo. A su vez, cada uno de estos corazones es una bomba bicameral pulsátil formada por una aurícula y un ventrículo.
Cada una de las aurículas es una bomba débil de cebado del ventrículo, que contribuye a transportar sangre hacia el ventrículo correspondiente. Los ventrículos después después aportan la principal fuerza del bombeo que impulsa la sangre: 1)hacia la circulación pulmonar por el ventrículo derecho, o 2) hacia la circulación sistémica por el ventrículo izquierdo.
FISIOLOGÍA DEL MÚSCULO CARDÍACO
El corazón está formado por tres tipos principales de músculo cardíaco: músculo auricular, músculo ventricular y fibras musculares especializadas de excitación y de conducción. El músculo auricular y ventricular se contrae de manera muy similar al músculo esquelético, excepto porque la duración de la contracción es mucho mayor. No obstante, las fibras especializadas de excitación y de conducción del corazón se contraen solo débilmente porque contienen pocas fibrillas contráctiles; en cambio, presentan descargas eléctricas rítmicas automáticas en forma de potenciales de acción o conducción de los potenciales de acción por todo el corazón, formando así un sistema excitador que controla el latido rítmico cardíaco.
EL MÚSCULO CARDÍACO ES UN SINCITIO.
Las zonas oscuras que atraviesan las fibras musculares cardíacas se denominan discos intercalados; realmente son membranas celulares que separan las células musculares cardíacas individuales entre sí. Es decir, las fibras musculares cardíacas están formadas por muchas células individuales conec
tadas entre sí en serie y en paralelo. En cada uno de los discos intercalados las membranas celulares se fusionan entre sí para formar uniones «comunicantes» (en hendidura) permeables que permiten una rápida difusión.
Desde un punto de vista funcional los iones se mueven con facilidad en el líquido intracelular a lo largo del eje longitudinal de las fibras musculares cardíacas, de modo que los potenciales de acción viajan fácilmente desde una célula muscular cardíaca a la siguiente, a través de los discos intercalados. Por tanto, el músculo cardíaco es un sincitio de muchas células musculares cardíacas en el que las células están tan interconectadas entre sí que cuando una célula se excita el potencial de acción se propaga rápidamente a todas.
El corazón realmente está formado por dos sincitios: el sincitio auricular, que forma las paredes de las dos aurículas, y el sincitio ventricular, que forma las paredes de los dos ventrículos. Las aurículas están separadas de los ventrículos por tejido fibroso que rodea las aberturas de las válvulas aurículoventriculares (AV) entre las aurículas y los ventrículos. Normalmente los potenciales no se conducen desde el sincitio auricular hacia el sincitio ventricular directamente a través de este tejido fibroso. Por el contrario, solo son conducidos por medio de un sistema de conducción especializado denominado haz AV, que es un fascículo de fibras de conducción de varios milímetros de diámetro.
POTENCIALES DE ACCIÓN EN EL MÚSCULO CARDÍACO.
El potencial de acción que se registra en una fibra muscular ventricular, que se muestra en la, es en promedio de aproximadamente 105 mV, lo que significa que el potencial intracelular aumenta desde un valor muy negativo, de aproximadamente –85 mV, entre los latidos hasta un valor ligeramente positivo, de aproximadamente +20 mV, durante cada latido. Después de la espiga inicial la membrana permanece despolarizada durante aproximadamente 0,2 s, mostrando una meseta, seguida al final de la meseta de una repolarización súbita. La presencia de esta meseta del potencial de acción ha- ce que la contracción ventricular dure hasta 15 veces más en el músculo cardíaco que en el músculo esquelético.
¿QUÉ PRODUCE EL POTENCIAL DE ACCIÓN PROLONGADO Y LA MESETA?
En el músculo cardíaco, el potencial de acción está producido por la apertura de dos tipos de canales: 1) los mismos canales rápidos de sodio activados por el voltaje que en el músculo esquelético y 2) otra población totalmente distinta de canales de calcio de tipo L (canales lentos de calcio), que también se denominan canales de calcio-sodio.
RESUMEN DE LAS FASES DEL POTENCIAL DE ACCIÓN DEL MÚSCULO CARDÍACO.
Fase 0 (despolarización), los canales de sodio rápidos se abren. Cuando la célula cardíaca es estimulada y se despolariza, el potencial de membrana se hace más positivo. Los canales de sodio activados por el voltaje (canales de sodio rápidos) se abren y permiten que el sodio circule rápidamente hacia el interior de la célula y la despolarice. El potencial de membrana alcanza +20 mV aproximadamente antes de que los canales de sodio se cierren.
Fase 1 (repolarización inicial), los canales de sodio rápidos se cierran. Los canales de sodio se cierran, la célula empieza a repolarizarse y los iones potasio salen de la célula a través de los canales de potasio.
Fase 2 (meseta), los canales de calcio se abren y los canales de potasio rápidos se cierran. Tiene lugar una breve repolarización inicial y el potencial de acción alcanza una meseta como consecuencia de: 1) una mayor permeabilidad a los iones calcio, y 2) la disminución de la permeabilidad a los iones potasio.
Fase 3 (repolarización rápida), los canales de calcio se cierran y los canales de potasio lentos se abren. El cierre de los canales iónicos de calcio y el aumento de la permeabilidad a los iones potasio, que permiten que los iones potasio salgan rápidamente de la célula, pone fin a la meseta y devuelve el potencial de membrana de la célula a su nivel de reposo.
Fase 4 (potencial de membrana de reposo) con valor medio aproximado de -90 mV.
VELOCIDAD DE LA CONDUCCIÓN DE LAS SEÑALES EN EL MÚSCULO CARDÍACO.
La velocidad de la conducción de la señal del potencial de acción excitador a lo largo de las fibras musculares auriculares y ventriculares es de unos 0,3 a 0,5 m/s, o aproximadamente 1/250 de la velocidad en las fibras nerviosas grandes y en torno a 1/10 de la velocidad en las fibras musculares esqueléticas. La velocidad de conducción en el sistema especializado de conducción del corazón, en las fibras de Purkinje, es de hasta 4 m/s.
PERIODO REFRACTARIO DEL MÚSCULO CARDÍACO
El período refractario normal del ventrículo es de 0,25 a 0,30 s, que es aproximadamente la duración del potencial de acción en meseta prolongado, Hay un período relativo refractario adicional de aproximadamente 0,05 s, durante el cual es más difícil de lo normal excitar el músculo pero, sin embargo, se puede excitar con una señal excitadora muy intensa.
ACOPLAMIENTO EXCITACIÓN-CONTRACCIÓN: FUNCIÓN DE LOS IONES CALCIO Y DE LOS TÚBULOS TRANSVERSOS.
El término «acoplamiento excitación-contracción» se refiere al mecanismo mediante el cual el potencial de acción hace que las miofibrillas del músculo se contraigan. Una vez más hay diferencias en este mecanismo en el músculo cardíaco que tienen efectos importantes sobre las características de su contracción. Al igual que en el músculo esquelético, cuando un potencial de acción pasa sobre la membrana del músculo cardíaco el potencial de acción se propaga hacia el interior de la fibra muscular cardíaca a lo largo de las membranas de los túbulos transversos (T). Los potenciales de acción de los túbulos T, a su vez, actúan sobre las membranas de los túbulos sarcoplásmicos longitudinales para producir la liberación de iones calcio hacia el sarcoplasma muscular desde el retículo sarcoplásmico. En algunas milésimas de segundo más estos iones calcio difunden hacia las miofibrillas y catalizan las reacciones químicas que favorecen el deslizamiento de los filamentos de actina y de miosina entre sí, lo que da lugar a la contracción muscular.
El calcio que entra en la célula activa después los canales de liberación de calcio, también denominados canales de receptor de rianodina, en la membrana del retículo sarcoplásmico, para activar la liberación de calcio en el sarcoplasma.
CICLO CARDÍACO.
Cada ciclo es iniciado por la generación espontánea de un potencial de acción en el nódulo sinusal. Este nódulo está localizado en la pared superolateral de la aurícula derecha, cerca del orificio de la vena cava superior, y el potencial de acción viaja desde aquí rápidamente por ambas aurículas y después a través del haz AV hacia los ventrículos. Las aurículas actúan como bombas de cebado para los ventrículos, y los ventrículos a su vez proporcionan la principal fuente de potencia para mover la sangre a través del sistema vascular del cuerpo.
DIÁSTOLE Y SÍSTOLE.
El ciclo cardíaco está formado por un período de relajación que se denomina diástole, seguido de un período de contracción denominado sístole. La duración del ciclo cardíaco total, incluidas la sístole y la diástole, es el valor inverso de la frecuencia cardíaca. Por ejemplo, si la frecuencia cardíaca es de 72 latidos/min, la duración del ciclo cardíaco es de 1/72 min/latido, aproximadamente 0,0139 min por latido, o 0,833 s por latido.
RELACIÓN DEL ELECTROCARDIOGRAMA CON EL CICLO CARDÍACO.
Son los voltajes eléctricos que genera el corazón, y son registrados mediante el electrocardiógrafo desde la superficie del cuerpo. La onda P está producida por la propagación de la despolarización en las aurículas, y es seguida por la contracción auricular, que produce una ligera elevación de la curva de presión auricular inmediatamente después de la onda P electrocardiográfica. Aproximadamente 0,16 s después del inicio de la onda P, las ondas QRS aparecen como consecuencia de la despolarización eléctrica de los ventrículos, que inicia la contracción de los ventrículos y hace que comience a elevarse la presión ventricular. Por tanto, el complejo QRS comienza un poco antes del inicio de la sístole ventricular. Finalmente, la onda T ventricular representa la fase de repolarización de los ventrículos, cuando las fibras del músculo ventricular comienzan a relajarse. Por tanto, la onda T se produce un poco antes del final de la contracción ventricular.
FUNCIÓN DE LAS AURÍCULAS COMO BOMBAS DE CEBADO PARA LOS VENTRÍCULOS
La sangre normalmente fluye de forma continua desde las grandes ventas hacia las aurículas; aproximadamente el 80% de la sangre fluye directamente a través de las aurículas hacia los ventrículos incluso antes de que se contraigan las aurículas. Después, la contracción auricular habitualmente produce un llenado de un 20% adicional de los ventrículos. Por tanto, las aurículas actúan como bombas de cebado que aumentan la eficacia del bombeo ventricular hasta un 20%. Sin embargo, el corazón puede seguir funcionando en la mayor parte de las condiciones incluso sin esta eficacia de un 20% adicional porque normalmente tiene la capacidad de bombear entre el 300 y el 400% más de sangre de la que necesita el cuerpo en reposo. Por tanto, cuando las aurículas dejan de funcionar es poco probable que se observe esta diferencia salvo que la persona haga un esfuerzo; en este caso de manera ocasional aparecen síntomas agudos de insuficiencia cardíaca, especialmente disnea.
DESBORDAMIENTO DE LOS VENTRÍCULOS DURANTE LA SÍSTOLE
Es el llamado período de contracción isovolumétrica o isométrica, lo que quiere decir que se produce aumento de la tensión en el músculo cardíaco, pero con un acortamiento escaso o nulo de las fibras musculares.
PERIODO DE EYECCIÓN
Cuando la presión ventricular izquierda aumenta ligeramente por encima de 80 mmHg (y la presión ventricular derecha ligeramente por encima de 8 mmHg), las presiones ventriculares abren las válvulas semilunares. Inmediatamente comienza a salir la sangre de los ventrículos. Aproximadamente el 60% de la sangre del ventrículo al final de la diástole es expulsada durante la sístole; en torno al 70% de esta porción es expulsado durante el primer tercio del período de eyección y el 30% restante del vaciado se produce durante los dos tercios siguientes. El primer tercio se denomina período de eyección rápida y los dos tercios finales período de eyección lenta.
PERIODO DE RELAJACIÓN ISOVOLUMÉTRICA (ISOMÉTRICA)
Las presiones elevadas de las grandes arterias distendidas que se acaban de llenar con la sangre que procede de los ventrículos que se han contraído empujan inmediatamente la sangre de nuevo hacia los ventrículos, lo que cierra súbitamente las válvulas aórtica y pulmonar. Durante otros 0,03 a 0,06 s el músculo cardíaco sigue relajándose, aun cuando no se modifica el volumen ventricular, dando lugar al período de relajación isovolumétrica o isométrica.
LAS VÁLVULAS CARDÍACAS EVITAN EL FLUJO INVERSO DE LA SANGRE DURANTE LA SÍSTOLE.
VÁLVULAS AURÍCULOVENTRICULARES.
Las válvulas AV (las válvulas tricúspide y mitral) impiden el flujo retrógrado de sangre desde los ventrículos hacia las aurículas durante la sístole, y las válvulas semilunares (es decir, las válvulas aórtica y de la arteria pulmonar) impiden el flujo retrógrado desde las arterias aorta y pulmonar hacia los ventrículos durante la diástole. Por motivos anatómicos, las válvulas AV, que están formadas por una película delgada, casi no precisan ningún flujo retrógrado para cerrarse, mientras que las válvulas semilunares, que son mucho más fuertes, precisan un flujo retrógrado bastante rápido durante algunos milisegundos.
VÁLVULAS AÓRTICA Y DE LA ARTERIA PULMONAR.
Las válvulas semilunares aórtica y pulmonar funcionan de una manera bastante distinta de las válvulas AV. Primero, las elevadas presiones de las arterias al final de la sístole hacen que las válvulas semilunares se cierren súbitamente, a diferencia del cierre mucho más suave de las válvulas AV. Segundo, debido a sus orificios más pequeños, la velocidad de la eyección de la sangre a través de las válvulas aórtica y pulmonar es mucho mayor que a través de las válvulas AV, que son mucho mayores.
CURVA DE PRESIÓN AÓRTICA.
La entrada de sangre en las arterias durante la sístole hace que sus paredes se distiendan y que la presión aumente hasta aproximadamente 120 mmHg. Se produce una incisura en la curva de presión aórtica cuando se cierra la válvula aórtica; está producida por un corto período de flujo retrógrado de sangre inmediatamente antes del cierre de la válvula, seguido por la interrupción súbita del flujo retrógrado.
Antes de que se contraiga de nuevo el ventrículo, la presión aórtica habitualmente ha disminuido hasta aproximadamente 80 mmHg (presión diastólica), que es dos tercios de la presión máxima de 120 mmHg (presión sistólica) que se produce en la aorta durante la contracción ventricular. Las curvas de presión del ventrículo derecho y de la arteria pulmonar son similares a las de la aorta, excepto que las presiones tienen una magnitud de solo aproximadamente 1/6.
<> DURANTE EL CICLO CARDÍACO: TRABAJO CARDÍACO.
Fase I: período de llenado. La fase I del diagrama volumen-presión comienza a un volumen ventricular de aproximadamente 50 ml y una presión diastólica próxima a 2 a 3 mmHg. La cantidad de sangre que queda en el ventrículo después del latido previo, 50 ml, se denomina volumen telesistólico.
Fase II: período de contracción isovolumétrica. Durante la contracción isovolumétrica el volumen del ventrículo no se modifica porque todas las válvulas están cerradas. Sin embargo, la presión en el interior del ventrículo aumenta hasta igualarse a la presión que hay en la aorta, hasta un valor de presión de aproximadamente 80 mmHg.
Fase III: período de eyección. Durante la eyección la presión sistólica aumenta incluso más debido a una contracción aún más intensa del ventrículo. Al mismo tiempo, el volumen del ventrículo disminuye porque la válvula aórtica ya se ha abierto y la sangre sale del ventrículo hacia la aorta.
Fase IV: período de relajación isovolumétrica. Al final del período de eyección se cierra la válvula aórtica, y la presión ventricular disminuye de nuevo hasta el nivel de la presión diastólica. La línea marcada como «IV» refleja esta disminución de la presión intraventricular sin cambios de volumen. Así, el ventrículo recupera su valor inicial, en el que quedan aproximadamente 50 ml de sangre en el ventrículo y la presión auricular es de aproximadamente de 2 a 3 mmHg. El área que encierra este diagrama volumen-presión funcional (la zona sombreada denominada TE) representa el trabajo cardíaco externo neto del ventrículo durante su ciclo de contracción.
CONCEPTOS DE PRECARGA Y POSCARGA.
Cuando se evalúan las propiedades contráctiles del músculo es importante especificar el grado de tensión del músculo cuando comienza a contraerse, que se denomina precarga y especificar la carga contra la que el músculo ejerce su fuerza contráctil, que se denomina poscarga. La precarga es la presión telediastólica cuando el ventrículo ya se ha llenado. La poscarga del ventrículo es la presión de la aorta que sale del ventrículo. La importancia de los conceptos de precarga y poscarga es que en muchos estados funcionales anormales del corazón o de la circulación, la presión durante el llenado del ventrículo (la precarga), la presión arterial contra la que se debe contraer el ventrículo (la poscarga) o ambas están alteradas con respecto a su situación normal en un grado importante.
EFECTO DE LA TEMPERATURA SOBRE LA FUNCIÓN CARDÍACA.
El aumento de la temperatura corporal, como ocurre durante la fiebre, produce un gran aumento de la frecuencia cardiaca, a veces hasta el doble del valor normal. El descenso de la temperatura produce una gran disminución de la frecuencia cardiaca, que puede disminuir hasta solo algunos latidos por minuto cuando una persona esta cerca de la muerte por hipotermia en el intervalo de temperatura corporal de 16 a 21 grados centígrados.
Brandon nazario vazquez balanzar
Excitación y contracción del musculo liso
Contracción del musculo liso
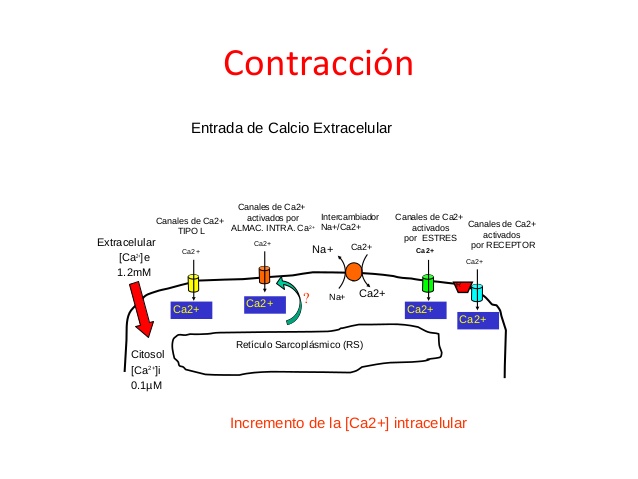
Muchos de los principios de la contracción que se aplican al musculo esquelético se aplican también al musculo liso y, lo que es más importante, esencialmente, las mismas fuerzas de atracción entre los filamentos de miosina y actina producen la contracción en el musculo liso, pero la disposición física interna de los filamentos de miosina y actina en las fibras musculares lisas es distintas de la encontrada en el musculo esquelético.
Tipos de músculos liso
En general, el musculo liso se puede dividir en dos tipos principales
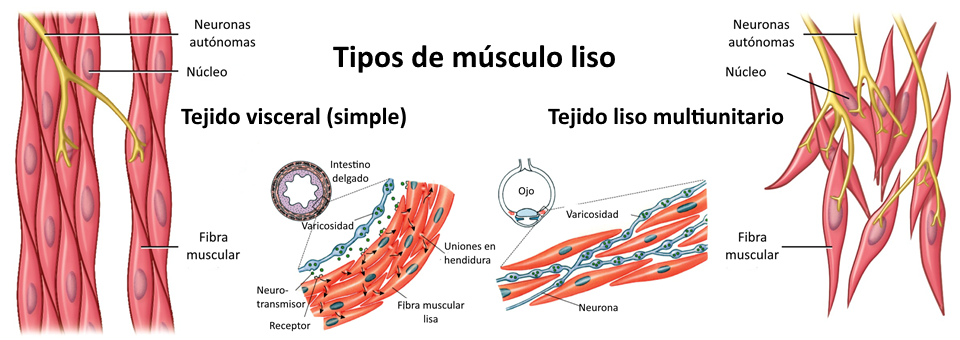
. Musculo liso multiunitario: las características más importantes de las fibras musculares lisas multiunitarias es que una de las fibras se pueda contraer independientemente de las demás, y su control se ejerce principalmente por señales nerviosas. Algunos ejemplos de musculo liso multiunitario son el musculo de los ojos musculo ciliar, el musculo del iris y los musculos piloerectores que producen la erección del pelo cuando los estimula el sistema nervioso simpático.
. musculo liso unitario: se denominan también musculo liso unitario, musculo liso sincital y musculo liso visceral, una masa de cientos a miles de fibras musculares lisas se contraen juntas como una única unidad. Las membranas celulares de fibras adyacentes están conectadas eléctricamente por uniones en hendidura, lo que permite que los potenciales de acción viajan desde una fibra a otra y que las fibras musculares se contraigan todas juntas. Este tipo de musculo se encuentra en las paredes del tubo digestivo, vías biliares, uréteres, útero, trompas de Falopio y vasos sanguíneos.
Base física de la contracción del musculo liso
El musculo liso tiene la misma disposición estriada de los filamentos de actina y miosina que se encuentran en el musculo esquelético.
Los filamentos de actina están unidos a los cuerpos. Algunos de estos cuerpos están dispersos en el interior de las células y se mantienen en su posición unidos entre si por un andamio de estructuras proteicas. Otros están unidos a la membrana celular y forman enlaces con los cuerpos densos de las células adyacentes, lo que permite que la fuerza de contracción se transmitan de unas células a otras. Por tanto, los cuerpos densos tienen una función similar a los discos Z en el musculo esquelético.
Los filamentos de miosina están entremezclados entre los de actina. Los filamentos de miosina presentan un diámetro más de dos veces mayor que los de actina.
Unidades contráctiles. Las unidades contráctiles individuales consisten en filamentos de actina que irradian desde dos cuerpos densos; dichos filamentos se superponen a un único filamento de miosina que está localizado a mitad de camino entre los cuerpos densos.
Comparación de la contracción del musculo liso con la contracción del musculo estriado
A diferencia de las contracciones del musculo del musculo esquelético las contracciones del musculo liso son contracciones tónicas prolongadas que a veces duran horas o incluso días. Las características físicas y químicas de la contracción del musculo liso son diferentes de las del musculo esquelético. A continuación se presentan algunas diferencias.
Ciclado lento de los puntos cruzados. La rapidez del ciclado de los puntos transversos en el musculo liso es mucho más lenta que en el musculo esquelético.
Baja densidad de energía. Para mantenerse la misma tensión de contracción en el musculo liso que en el musculo esquelético solo es necesario de 1/10 a 1/300 de energía.
Lentitud del inicio de la contracción y relajación. Un tejido muscular liso típico comienza a contraerse de 50 a 100 ms después de ser excitado y tiene un tiempo total de contracción de 1 a 3 s. este tiempo es aproximadamente 30 veces más prolongado que en una fibra muscular esquelética media.
Aumento de la fuerza máxima de contracción. La fuerza máxima de contracción del musculo liso por unidad de sección transversal del musculo es, con frecuencia, mayor que la del musculo esquelético. Esta gran fuerza de contracción del musculo liso se debe al periodo prolongado de unión de los puentes cruzados de miosina a los filamentos de actina.
El acortamiento porcentual del musculo liso es mayor que el del musculo esquelético. El musculo esquelético tiene una distancia útil de contracción de solo un tercio a una cuarta parte de su longitud en reposo, mientras que el musculo liso puede contraerse más de dos tercios de su longitud estirado. El mecanismo de cerrojo facilita el mantenimiento prolongado de las contracciones. Una vez que el musculo liso ha generado la contracción máxima, la magnitud de la excitación continuada puede reducirse normalmente muy por debajo del nivel inicial, a pesar de lo cual el musculo mantiene su fuerza de contracción completa. Esto se denomina mecanismo de cerrojo. La importancia del mecanismo de cerrojo es que permite mantener durante horas una contracción tónica prolongada en el musculo liso con un bajo consumo de energía.
Regulación de la contracción por los iones calcio
Los iones calcio se combinan con la calmodulina para provocar la activación de la miosina cinasa y la fosforilacion de la cabeza de la miosina. En lugar de la troponina, las células musculares lisas contienen otra proteína reguladora de unión al calcio denominada calmodulina. Aunque esta proteína reacciona con los iones de calcio, se diferencia de la troponina en la forma en que inicia la contracción, ya que lo hace activando los puentes cruzados de miosina. Por tanto, la regulación de la contracción se basa en la miosina en el musculo liso y no en la actina como en el musculo esquelético. Esta activación y la posterior contracción se producen según las siguientes secuencias:
Los iones calcio se unen a la calmodulina; el complejo calmodulina-calcio se une después de la miosina cinasa, que es una enzima fosforiladora.
Una de las cadenas ligeras de cada una de las cabezas de miosina, denominada cabeza reguladora, se fosforila en respuesta a esta miosina cinasa.
Cuando esta cadena esta fosforilada la cabeza tiene la capacidad de unirse al filamento de actina, produciendo la contracción muscular. Cuando esta cadena ligera de miosina no está fosforilada no se produce el ciclo de unión-separación de la cabeza de miosina con el filamento de actina
La miosina fosfatasa es necesaria en la interrupción de la contracción. Cuando la concentración de los iones de calcio disminuye por debajo de su nivel cítrico, los procesos que se acaban de señalar se invierten automáticamente, excepto la fosforilacion de la cabeza de la miosina. La inversión de esta reacción precisa otra enzima, la miosina fosfatasa, que escinde el fosfato de la cadena liguera reguladora; entonces se interrumpe el ciclo y se produce la relajación.
Control nervioso y hormonal de la contracción del musculo liso
Uniones neuromusculares del musculo liso
Las uniones neuromusculares del tipo muy estructurado que se encuentra en las fibras del musculo esquelético no aparecen en el musculo liso.
Uniones difusas: son los lugares de secreción de las sustancias transmisoras. En la mayoría de los casos, las fibras nerviosas autónomas forman las denominadas uniones difusas, que segregan su neurotransmisor en la matriz que recubre el musculo liso, desde donde difunden una corta distancia hacia las fibras.
Varicosidades de los terminales de axones. Los axones que inervan las fibras musculares lisas no tienen los extremos terminales ramificados típicos que se ven en la placa motora terminal de las fibras musculares esqueléticas. Por el contrario, la mayoría de los axones terminales delgados tienen múltiples varicosidades distribuidas a lo largo de sus ejes. Las varicosidades contienen vesículas cargadas con la sustancia neurotransmisora.
Uniones de contacto. En el musculo liso tipo multiunitario las varicosidades se encuentran directamente sobre la membrana de la célula muscular. Las llamadas uniones de contacto actúan de manera muy similar a las uniones neuromusculares del musculo esquelético.
La acetilcolina y la noradrenalina pueden tener efectos excitadores o inhibidores en la unión neuromuscular del musculo liso. La acetilcolina y la noradrenalina son secretadas por las mismas neuronas. La acetilcolina es una sustancia transmisora excitadora de las fibras musculares lisas en algunos órganos, pero es un transmisor inhibidor en el musculo liso en otros. Cuando la acetilcolina excita una fibra muscular, la noradrenalina habitualmente la inhibe y viceversa.
Potenciales de membrana y potenciales de acción en el musculo liso.
El potencial de membrana en reposo depende del tipo de musculo liso y de la situación momentánea del musculo. Normalmente es de alrededor de -50 a -60 mV, o aproximadamente a -30 mV menos negativo que en el musculo esquelético.
Los potenciales de acción se producen en le musculo lioso unitario, como el musculo visceral, de la misma manera que en el musculo esquelético. Los principales potenciales de acción del musculo liso visceral se producen en dos formas:
Potenciales en espiga. Los potenciales de acción en espiga típicos aparecen en la mayor parte de los tipos de musculo liso unitario. Se pueden generar mediante estimulación eléctrica, por distensión o como consecuencias de la acción de hormonas y sustancias transmisoras, o pueden a ser el resultado de la generación espontánea en la propia fibra muscular.
Potenciales de acción con meseta. El inicio de este potencial de acción es similar al del potencial en espiga típico. Sin embrago, la repolarización se retrasa durante varios cientos de milisegundos. Esta meseta puede ser responsables de la contracción prolongada que se produce en el uréter, en el útero en algunas situaciones y en ciertos tipos de músculos liso vascular.
Los canales de calcio son necesarios en la generación del potencial de acción del musculo liso. El sodio participa poco en la generación del potencial de acción en la mayor parte del musculo liso. Por ek contrario, el movimiento de iones calcio hacia el interior de la fibra es el principal responsable del potencial de acción.
Causa de las ondas lentas. Dos causa posibles de las ondas lentas son las oscilaciones de la actividad de la bomba de sodio, que hacen que el potencial de acción se más negativo cuando el sodio se bombea rápidamente, y menos negativo cuando la bomba de sodio es menos activa, y las conductancias de los canales iónicos, que aumentan y disminuyen de manera rítmica.
Importancia de las ondas lentas. Cuando el potencial de las ondas lentas aumenta por encima de cierto umbral pueden iniciar potencial de acción. El potencial de acción se propaga a lo largo de la masa muscular y se produce la contracción. Las ondas lentas de por sí pueden provocar contracciones musculares en el musculo liso gástrico.
Los potenciales de acción espontáneos se generan por la distensión del musculo liso visceral. Los potenciales de acción espontáneos son consecuencias de una combinación de potenciales de onda lenta normales añadidos a una disminución de la negativa global del potencial de membrana que produce la propia distensión. Esta respuesta a la distensión permite que la pared del tubo digestivo, cuando se distiende excesivamente, se contraiga automáticamente, resistiéndose a la tensión
Efectos de los factores tisulares locales y las hormonas en la contracción del musculo liso sin potenciales de acción.
Contracción del musculo liso en respuestas a factores químicos tisulares locales. Esta respuesta vasodilatadora es necesaria para el control local del flujo sanguíneo. Muchas hormonas circulantes en la sangre afectan en cierto grado a la contracción del musculo liso. Una hormona produce contracción del musculo liso cuando la membrana de la célula muscular contiene receptores excitadores activados por hormonas para la hormona respectiva. Por el contrario, la hormona produce relajación si la membrana contiene receptores inhibidores.